
今有0.1mol/L Na2SO4溶液300mL,0.1mol/L MgSO4溶液200mL和0.1mol/L Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子浓度之比是( )
A 1:1:1 B 3:2:1 C 3:2:3 D 1:1:3
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分子化合物PVB的合成路线如下:

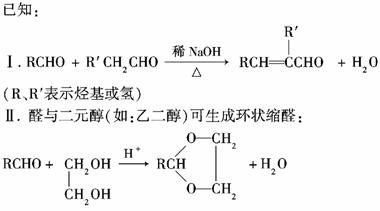
(1)A的核磁共振氢谱有两种峰,A的名称是________。
(2)A与  合成B的化学方程式是__________________________。
合成B的化学方程式是__________________________。
(3)C为反式结构,由B 还原得到。C的结构简式是
______________________________________________________________________ __。
__。
(4)E能使Br2的CCl4溶液褪色。N由A经反应①~③合成。
a.①的化学试剂和条件是___________________________________ ___。
___。
b.②的反应类型是_____________________________________________。
c.③的化学方程式是__________________________________________________。
(5)PVAc由一种单体经加聚反应得到,该单体的结构简式是____________________。
(6)碱性条件下,PVAc完全水解的化学方程式是__________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施,是为了防止产生雾霾的,其中不可行的是( )
A.停止冬季供暖,减少有害物质排放
B.对锅炉和汽车等产生的有害气体和烟尘等进行处理
C.退耕还林,改善生态环境
D.寻找新能源,减少化石燃料的使用
查看答案和解析>>
科目:高中化学 来源: 题型:
密度为1.84g/cm3,浓度为98%的浓H2SO4的物质的量的浓度为( )
A.18.4mol/L B.9.2mol/L C.13mol/L D.12mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空:
(1)Fe(OH)2在空气中变质的化学方程为: 。
(2)漂白粉在空气中久置会变质,变质过程中既有非氧化还原反应又有氧化还原反应,其中氧化还原反应的方程式为: 。
(3)实验室制备氨气的反应方程式为: ,收集氨气时,在试管口放一小团棉花其作用是 ,用 试纸检验氨气是否收集满。
(4)将CaMg3Si4O12改写为氧化物的形式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池的电池反应为:Fe+2Fe3+===3Fe2+ ,与此电池反应不符的原电池是
,与此电池反应不符的原电池是
A.铜片、铁片、FeCl3溶液组成的原电池
B.石墨、铁片、Fe(NO3)3溶液组成的原电池
 C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
D.铜片、铁片、Fe(NO3)3溶液组成的原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在能源开发与利用中起着十分关键的作用。氢气是一种新型的绿色能源,又是一种重要的化工原料。
Ⅰ.氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行如图所示的实验(图中所用电极均为惰性电极):

(1)对于氢氧燃料电池,下列叙述不正确的是________。
A.a电极是负极,OH-移向负极
B.b电极的电极反应为:O2+2H2O+4e-===4OH-
C.电池总反应式为:2H2+O2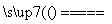 2H2O
2H2O
D.电解质溶液的pH保持不变
E.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(2)上图右边装置中盛有100 mL 0.1 mol·L-1AgNO3溶液,当氢氧燃料电池中消耗氢气112 mL(标准状况下)时,此时AgNO3溶液的pH=________(溶液体积变化忽略不计)。
Ⅱ.已知甲醇的燃烧热ΔH=-726.5 kJ·mol-1,在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为_________________________________________________________,
正极的反应式为_________________________ __________________________________。
__________________________________。
理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为______________________________ __________________________________________
__________________________________________
(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作完全正确的是( )
| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液1000 mL | 准确称取氯化钾固体,放入到1000 mL的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | Fe(OH)3胶体的制备 | 向沸水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com