
����Ŀ�������������壨FeSO47H2O����ҽҩ������Ѫ����ij�����о�С��ⶨ�ò�Ѫ������Ԫ�صĺ�����ʵ�鲽�����£� 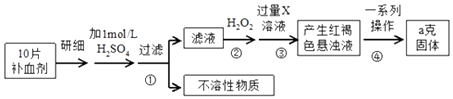
��ش��������⣺
��1��֤���������Һ�к���Fe2+�ķ������ȵμ�KSCN��Һ���ٵμ� �� �ù��̵�����Ϊ�� ��
��2������ڼ������H2O2��Ŀ�ģ� ��
��3��������з�Ӧ�����ӷ���ʽ�� ��
��4����ʵ������ģ���ÿƬ��Ѫ������Ԫ�ص�����g��
��5����С����Щͬѧ��Ϊ��KMnO4��Һ�ζ�Ҳ�ܽ�����Ԫ�غ����IJⶨ��
��5Fe2++MnO4��+8H+=5Fe3++Mn2++4H2O��
��ʵ��ǰ������Ҫ��ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ����������ƽ���������ձ�����ͷ�ι��⣬���� ��
������ʵ���е�KMnO4��Һ��Ҫ�ữ�������ữ������ ��
a��ϡ���� b��ϡ���� c��ϡ���� d��Ũ����
�۵ζ����յ�ʱ����ɫΪɫ�����ζ����յ�ʱ���ӵζ��̶ܿ��ߣ��Բ���ֵ�к�Ӱ�죿�� �ƫ�ߡ�ƫ�ͻ���Ӱ�족����
���𰸡�
��1����ˮ����˫��ˮ��ϡ���ᣩ����Һ��ʼ����ɫ�����ΪѪ��ɫ
��2����Fe2+ȫ������ΪFe3+
��3��Fe3++3NH3?H2O�TFe��OH��3��+3NH4+
��4��0.07a
��5��250mL����ƿ��b���ϻ��Ϻ죻ƫ��
���������⣺��1��Fe3+��KSCN��Һ�Ժ�ɫ�����������ڼ���Fe3+���ڣ����Լ�����������Fe2+����ΪFe3+����Fe2+ �� �����ȵμ�KSCN��Һ����Һ����ɫ��������ˮ����˫��ˮ��ϡ���ᣩ������2Fe2++Cl2�T2Fe3++2Cl�� �� ��Һ��ΪѪ��ɫ������Fe3++3SCN��Fe��SCN��3 �� ˵������Fe2+ ��
���Դ��ǣ���ˮ����˫��ˮ��ϡ���ᣩ����Һ��ʼ����ɫ�����ΪѪ��ɫ����2��˫��ˮ���������ԣ������������ܽ�Fe2+ȫ������ΪFe3+ �� 2H++H2O2+2Fe2+=2Fe3++2H2O�����Դ��ǣ���Fe2+ȫ������ΪFe3+����3��������ǽ�Fe3+ת��Ϊ�����������������Լ��백ˮ����Ӧ���ӷ���ʽΪFe3++3NH3H2O�TFe��OH��3��+3NH4+ ��
���Դ��ǣ�Fe3++3NH3H2O�TFe��OH��3��+3NH4+����4��ag����������Ԫ�ص�������Ϊ10Ƭ��Ѫ������������������ÿƬ��Ѫ������Ԫ�ص����� ![]() =0.07ag�����Դ��ǣ�0.07a����5���پ�ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ����������ƽ��ҩ�ס��������ձ�����ͷ�ιܡ�250mL����ƿ�����Դ��ǣ�250mL����ƿ��
=0.07ag�����Դ��ǣ�0.07a����5���پ�ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ����������ƽ��ҩ�ס��������ձ�����ͷ�ιܡ�250mL����ƿ�����Դ��ǣ�250mL����ƿ��
�ڸ��������ǿ�����ԣ��ܽ�����������������������ԣ�������������������ֻ����ϡ�����ữ�����Դ��ǣ�b��
���ø��������Һ�ζ���������ʱ���ζ����յ�ʱ��Һ�������ɫ���Ϻ�ɫ�����ζ����յ�ʱ���ӵζ��̶ܿ��ߣ�������ĸ��������Һ�����ƫС�����Ի�ʹ����ֵƫ�ͣ�
���Դ��ǣ��ϻ��Ϻ죻ƫ�ͣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ȷ����
A. SO2�ڿ������ױ�����ΪSO3
B. �ڱ�״������SO3������Ħ�������22.4��
C. SO2 ��SO3������ˮ���ҷ�Ӧ
D. SO2������Ư��ֽ����SO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����������ᷴӦ����������������Һ��Ӧ���ǣ� ��
A.AlCl3
B.Al��OH��3
C.Al2��SO4��3
D.NaAlO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3.20g��Cu��50.0mL��10.0molL��1��HNO3��ַ�Ӧ����ԭ������NO��NO2 �� ����Ӧ����Һ����xmol H+ �� ���ʱ��Һ�к�NO3�������ʵ���Ϊ�� ��
A.![]() mol
mol
B.��x+0.1��mol
C.2x mol
D.0.1x mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NF3����һ�����͵��Ӳ��ϣ����ڳ�ʪ�Ŀ�������ˮ�����ܷ���������ԭ��Ӧ���䷴Ӧ�IJ����У�HF��NO��HNO3 �� �����Ҫ��ش��������⣺
��1����Ӧ�����У��������뱻��ԭ��Ԫ��ԭ�ӵ����ʵ���֮��Ϊ ��
��2��д���÷�Ӧ�Ļ�ѧ����ʽ �� ����Ӧ������0.2mol HNO3 �� ת�Ƶĵ�����ĿΪ����
��3��NF3��һ����ɫ���������壬��һ��NF3�ڿ�����й©���������ڷ��֣����жϸ�����й©ʱ�������� ��
��4��һ��NF3й©��������NaOH��Һ���ܵķ���������Ⱦ��������NaNO2��NaF��H2O�⣬���϶������ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ĸ����ݶ���ʾ�ϳɰ��ķ�Ӧ���ʣ��������ʴ���ͬһ��Ӧ�е��ǣ� �� ��V��N2��=0.6mol/��Lmin�� ��V��NH3��=1.8mol/��Lmin��
��V��H2��=1.2mol/��Lmin�� ��V��H2��=0.045mol/��Ls��
A.�٢�
B.�٢�
C.�ۢ�
D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɻ��õ������������泥�NH4ClO4���Ļ����Ϊ����ȼ�ϣ���ȼʱ����������������������立�Ӧ���䷽��ʽ�ɱ�ʾΪ��2NH4ClO4 ![]() N2��+4H2O+Cl2��+2O2�����ų�����ΪQ�����жԴ˷�Ӧ�����д�����ǣ� ��
N2��+4H2O+Cl2��+2O2�����ų�����ΪQ�����жԴ˷�Ӧ�����д�����ǣ� ��
A.��Ӧ���ڷֽⷴӦ
B.������Ӧ˲������������������ƶ�����ɻ�����
C.��Ӧ�������仯��˵����Ҫ�ǻ�ѧ��ת��Ϊ���ܺͶ���
D.�ڷ�Ӧ�и������ֻ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NF3����һ�����͵��Ӳ��ϣ����ڳ�ʪ�Ŀ�������ˮ�����ܷ���������ԭ��Ӧ���䷴Ӧ�IJ����У�HF��NO��HNO3 �� �����Ҫ��ش��������⣺
��1����Ӧ�����У��������뱻��ԭ��Ԫ��ԭ�ӵ����ʵ���֮��Ϊ ��
��2��д���÷�Ӧ�Ļ�ѧ����ʽ �� ����Ӧ������0.2mol HNO3 �� ת�Ƶĵ�����ĿΪ����
��3��NF3��һ����ɫ���������壬��һ��NF3�ڿ�����й©���������ڷ��֣����жϸ�����й©ʱ�������� ��
��4��һ��NF3й©��������NaOH��Һ���ܵķ���������Ⱦ��������NaNO2��NaF��H2O�⣬���϶������ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ���ʵ��������и�������ȫȼ�պ��������������ǣ� ��
A.����
B.����
C.��ϩ
D.��Ȳ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com