
����Ŀ����֪AΪ����ɫ���壬T��R Ϊ���ֳ�������;�㷺�Ľ������ʣ�D���д��Եĺ�ɫ���壬C����ɫ��ζ�����壬MΪ���ɫ���塣�ش��������
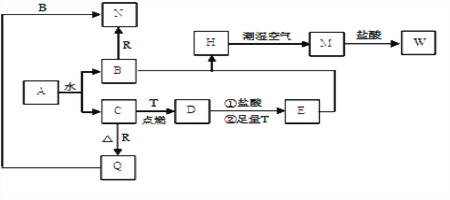
��1��д��D�Ļ�ѧʽ�� ____________
��2��д��A�ĵ���ʽ�� _____________
��3��H�ڳ�ʪ�����б�ΪM�������ǣ�______________��ѧ����ʽΪ�� ________________
��4��B��R��Ӧ�Ļ�ѧ����ʽΪ�� __________________________
��5�����ˮ�м���W������Һ�����Ƶ�һ�ֺ��ɫ��Һ�壬�����Һ�����ҺW�ļ�ʵ�鷽���� ____________________
���𰸡� Fe3O4 ![]() ���ɰ�ɫ��������Ϊ����ɫ������Ϊ���ɫ 4Fe(OH)2 + 2H2O+ O2 = 4Fe(OH)3 2Al+2NaOH+2H2O=2NaAlO2 +3H2�� ���������
���ɰ�ɫ��������Ϊ����ɫ������Ϊ���ɫ 4Fe(OH)2 + 2H2O+ O2 = 4Fe(OH)3 2Al+2NaOH+2H2O=2NaAlO2 +3H2�� ���������
�����������⿼��������ƶϣ�AΪ����ɫ���壬����ˮ��Ӧ����AΪNa2O2��CΪ��ɫ���壬��ΪO2��BΪNaOH��RΪ����������NaOH��Ӧ����RΪAl����NΪNaAlO2��D�Ǿ��д��Եĺ�ɫ���壬��DΪFe3O4��TΪFe��MΪFe(OH)3��WΪFeCl3����1������DΪ���Ժ�ɫ���壬��DΪFe3O4����2��AΪNa2O2�������ʽΪ��![]() ����3��Fe3O4Ͷ�뵽����������Fe2����Fe3�����ټ���Fe���ʣ�����Fe��2Fe3��=3Fe2������EΪFeCl2��HΪFe(OH)2���ڳ�ʪ�����з���4Fe(OH)2��O2��2H2O=4Fe(OH)3�����������ɰ�ɫ��״������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����4������2Al��2NaOH��2H2O=2NaAlO2��3H2������5�����ɫ��Һ���������������壬���������Һ�ļ����Ƕ����ЧӦ��������ж����ЧӦ����Һû�С�
����3��Fe3O4Ͷ�뵽����������Fe2����Fe3�����ټ���Fe���ʣ�����Fe��2Fe3��=3Fe2������EΪFeCl2��HΪFe(OH)2���ڳ�ʪ�����з���4Fe(OH)2��O2��2H2O=4Fe(OH)3�����������ɰ�ɫ��״������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����4������2Al��2NaOH��2H2O=2NaAlO2��3H2������5�����ɫ��Һ���������������壬���������Һ�ļ����Ƕ����ЧӦ��������ж����ЧӦ����Һû�С�


 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п�̸ɵ���ڵĺ�ɫ����ˮ�����̼������(��MnO2��C��Hg2+�ȣ���ȡMnSO4 H2O ��ʵ���������£�

��֪:25��ʱ������������ܶȻ���������:
���� | FeS | MnS | HgS |
�ܶȻ� | 5.0��l0-18 | 4.6��l0-14 | 2.2��l0-54 |
25��ʱ�����ֽ���������������������ʽ����ʱ��Һ��pH���±���ʾ:
������ | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
��ʼ������pH | 2.7 | 7.6 | 8.3 |
��ȫ������pH | 3.7 | 9.7 | 9.8 |
��1�����������У�����ʵ�����ʱ�õ��Ĺ����β��ʵ�������______________��
��2���ڼ��������¡���ȡ������ԭ����__________________����ȡʱ����MnSO4��Fe2(SO4)3�Ļ�ѧ����ʽΪ__________________________��
��3������I�ijɷ�ΪMnO2��C��____________(�ѧʽ��������ȡ��Ӧ��25��ʱ���У�FeS���������ֽ�ȡ����Һ�е�c(Hg2+)/C(Fe2+)= ____________(����ֵ����
��4����������ʱ�����ӷ���ʽΪ____________������ʱ����H2O2����MnO2��H2O2�ĵ���ʽΪ_______��
��5���к�ʱ��Ӧ�õ�����ҺpH�ķ�Χ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ؽ��IJ������ڹؽڻ�Һ���γ���������(NaUr)���壬�����ں��伾���շ��ؽ���ʹ���仯ѧ����Ϊ��
��HUr(����)��H2O![]() Ur��(���������)��H3O�� Ka(37��)��4.0��10��6
Ur��(���������)��H3O�� Ka(37��)��4.0��10��6
��Ur��(aq)��Na��(aq)![]() NaUr(s)
NaUr(s)
�ش��������⣺
��1�������¶ȣ�ƽ������ (����ҡ�����ͬ)�ƶ�������ˮϡ�ͣ�ƽ������ �ƶ���
��2��37��ʱ��1.0 Lˮ�������ܽ�8.0��10��3mol�����ƣ����¶��������Ƶ�KspΪ ��
��3���ؽ��������ڽ�ֺ����ָ�Ĺؽڴ�����Ϊ��Щ��λ���¶�һ��ϵ͡���˵���¶Ƚ���ʱ�������Ƶ�Ksp________(���������С�����䡱)��ע��ؽڵķ�����ů���ɻ���ؽ����µ���ʹ��˵����Ӧ������H 0(�>����<��)
��4��37��ʱ��ij�����ʯ������Һ��������Ӻ���������ӵ���Ũ��Ϊ2.50��10��3mol/L������������ӵ�Ũ��Ϊ5.00��10��4mol/L���ò�����Һ��pH= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� )
A. ��������������ʴʱ������ʴ�����ʺ�����Ũ����
B. ��״���£�2.24LCCl4�����й��ۼ�����ĿΪ0.4��6.02��1023
C. �����ʺϵ�����������Ӧ2Fe3++2I-=2Fe2++I2��Ƴ���ͼ��ʾ��ԭ��ء�������֭����Ϊ����ڼ�������FeCl2���壬������ʯī�缫Ϊ����

D. ��ʢ��2mL����H2S��Һ����֧�Թ��зֱ�μ�1��Ũ�Ⱦ�Ϊ0.1mol/L��ZnSO4��Һ��CuSO4��Һ����CuS���ɶ���ZnS���ɣ���Ksp(CuS)<Ksp(ZnS)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�뻷����������ҵ�����������������أ�����˵������ȷ���ǣ� ��
A. ��ʳƷ���з���װ�й轺�����۵���С�����ɷ�ֹʳ���ܳ�����������
B. ��SO2���������ԣ��ʿ�����Ư��ֽ��
C. ���챦ʯ��Ҫ�ɷ������������մɡ�����ɸ��Ҫ�ɷ��ǹ�����
D. �����Ƶ�ˮ��Һ�׳�ˮ���������Ʊ��轺��ľ�ķ������ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������з������Ʊ����壬�ܹ��õ��������
A. ��������������ʵ���Ũ�ȵ�BaCl2��Һ���������ϲ���
B. ��1 mL�������Ȼ�����Һ��μ��뵽20 mL��ˮ�У��ӱ��������ȵ�����
C. ��1 mL�������Ȼ�����Һһ���Լ��뵽20 mL��ˮ�У������Խ���
D. ��1 mL�������Ȼ�����Һ��μ��뵽20 mL��ˮ�У��ӱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������廯����X��Y���Ǵ����Կ�ֲ������ȡ�����ϡ�X�ɰ�����·�ߺϳ�Y��

��֪��

��1��X�Ĺ���������Ϊ__________________��
��2��Y�Ľṹ��ʽΪ_____________________��
��3��D+G��Y���л���Ӧ����Ϊ__________________��
��4���������ʲ�����D��Ӧ����_________��ѡ����ţ���
a�������� b�������� c��̼������Һ d������
��5��д�����з�Ӧ����ʽ��
X��G�ĵڢٲ���Ӧ______________________��
E��F______________________��
��6��G�ж���ͬ���칹�壬д��ͬʱ��������������G������ͬ���칹��Ľṹ��ʽ______________________��
i���ܷ���������Ӧ ii���ܷ���ˮ�ⷴӦ iii��������ֻ��һ��ȡ����
��7��G��һ��ͬ���칹��H�Ľṹ��ʽΪ![]() ��д����
��д����![]() Ϊ�л�ԭ�ϣ���ȡH�ĺϳ�·�ߣ�����ѡ��ԭ�ϣ���
Ϊ�л�ԭ�ϣ���ȡH�ĺϳ�·�ߣ�����ѡ��ԭ�ϣ���
![]()
![]() ______________________
______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�����Ӧ�õ�˵���д������
A. �轺��ƿװҩƷ�ĸ���� B. Һ������ҽ�������
C. С�մ����決ʳƷ�����ɼ� D. ��ʯӢ�������ڴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ˮ�г�����һ������ Cr2O72���� CrO42�������ǻ����̬ϵͳ�����ܴ���˺�����ҵ�϶Է�ˮ�����Ĺ�����������
![]()
��1��CrO4�� Cr �Ļ��ϼ� ��Cr3+�ĺ�������Ų�ʽΪ ��
��2��д�����������������ӷ�Ӧ����ʽ ���������£���Сƽ����ϵ�� pH �� pH=2������Һ�������� ɫ��
(3���������У���ԭ 0.01mol Cr2O72�����ӣ���Ҫ mol �� FeSO4��7H2O
��4����֪ Cr��OH��3 ����Һ�д�������ƽ�⣺H++CrO2-+H2O ![]() Cr��OH��3
Cr��OH��3![]() Cr3++3OH-�����й�˵������ȷ����
Cr3++3OH-�����й�˵������ȷ����
a���� HCl ��ƽ��������ƶ��������� Cr3+��
b���������ʷ��� Cr��OH��3 ������������������������
c��Cr3+������μ��� NaOH ��Һ���Ȳ����������������ʧ
d��Cr��OH��3 ������Һ��һ���� c(H )=c(OH )
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com