
分析 乙烯含有碳碳双键,可与溴水发生加成反应,可与水反应生成乙醇,可发生加聚反应和氧化反应,以此解答该题.
解答 解:(1)乙烯与溴发生加成反应生成1,2-二溴乙烷,反应方程式为CH2=CH2+Br2→CH2Br-CH2Br.
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;
(2)乙烯可与水发生加成反应生成,故答案为:CH3CH2OH; 加成;
(3)(A)乙烯含有碳碳双键,与溴的四氯化碳溶液发生加成反应,与酸性高锰酸钾溶液褪色发生氧化还原反应,故A错误;
(B)SO2具有还原性,与溴水和酸性高锰酸钾溶液褪色发生氧化还原反应,故B正确;
(C)SO2使品红溶液褪色,表现漂白性,具有酸性,可使滴有酚酞的NaOH溶液褪色,故C错误.
故答案为:(B).
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该类题目的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 所有的烷烃,彼此都是同系物 | |
| B. | 两种化合物的组成元素相同,各元素的质量分数也相同,二者一定具有相同最简式 | |
| C. | 组成元素的质量分数相同的不同化合物互为同分异构体 | |
| D. | 互为同系物的有机物相对分子质量一定相差14的整数倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水溶解后,向试管中加入足量稀硝酸 | 有气体产生,说明样品中含有Na2CO3 |
| ② | 向试管中加入足量Ba(NO3)2溶液 | 若有沉淀产生,则含Na2SO4,若没有沉淀产生,则不含Na2SO4 |
| ③ | 若②操作无沉淀,则向试管中加入0.1mol•L-1AgNO3溶液.若②操作中有沉淀,则将试管静置片刻后,取上层清液于另一去试管中,加入0.1mol•L-1AgNO3溶液 | 有沉淀产生,则含NaCl;无沉淀产生,则不含NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
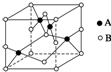 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子中,两个O之间形成2对共用电子对 | |
| B. | N2的电子式是N┇┇N | |
| C. | CO2和CS2都是直线型分子 | |
| D. | 白磷和甲烷都是正四面体型,键角都是109°28′ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,铝遇冷浓硝酸钝化 | B. | 浓盐酸的质量减轻 | ||
| C. | 澄清的石灰水变浑浊 | D. | 氢氧化钠固体发生潮解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com