
【题目】0.1mol下列气体分别与1L0.1mol·L-1的NaOH溶液反应,形成的溶液pH最小的是( )
A.NO2
B.SO2
C.SO3
D.CO2
科目:高中化学 来源: 题型:
【题目】下列关于过滤操作的说法中,错误的是( )
A. 玻璃棒下端要靠在三层滤纸处
B. 滤纸边缘低于漏斗边缘,多余部分要剪去,并用水润湿贴紧,不留气泡
C. 过滤时将液体沿玻璃棒注入过滤器,并使液面高于滤纸边缘
D. 漏斗下端紧靠烧杯内壁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.再加入10mL pH=11的NaOH溶液,混合液pH=7
C.醋酸的电离程度增大,c(H+)亦增大
D.溶液中 ![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空: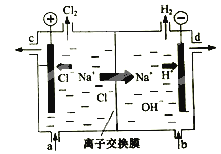
已知: H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7
HClO Ki1=2.95×10-8
H2CO3 Ki1=4.3×10-7 Ki2=5.6×10-11
(1)写出电解饱和食盐水的离子方程式。
(2)离子交换膜的作用为: 、 。
(3)精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中 位置流出。(选填“a”、“b”、“c”或“d”)
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2 , 还生成CO2和KHSO4等物质。
写出该反应的化学方程式
(5)室温下,0.1 mol/L NaClO溶液的pH 0.1 mol/L Na2SO3溶液的pH。(选填“大于”、“小于”或“等于”)。
浓度均为0.1 mol/L 的Na2SO3和Na2CO3的混合溶液中,SO32–、CO32–、HSO3–、HCO3– 浓度从大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事故处理措施正确的是
A. 实验用剩的试剂都不能放回原试剂瓶,以防污染试剂
B. 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度
C. 如果少量酒精失火燃烧,立即用水浇灭
D. 眼睛里溅进盐酸,立即用 NaOH 溶液洗涤眼睛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物中,核磁共振氢谱中出现三组峰,且峰面积之比为:2:2:1的是( )
A.CH3CH2CH2OH
B.CH3OCH3
C.CH2=CH﹣CH3
D.一氯苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究.在相同温度下,M的物质的量浓度(molL﹣1)随时间(min)变化的有关实验数据见表.下列说法不正确的是( )
时间 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.4 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.4 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Ca2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
A.在0~20 min内,Ⅰ中M的分解速率为0.015 molL﹣1min﹣1
B.水样酸性越强,M的分解速率越快
C.在0~20 min内,Ⅲ中M的分解百分率比Ⅱ大
D.由于Ca2+存在,Ⅳ中M的分解速率比Ⅰ快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com