
【题目】室温下向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.再加入10mL pH=11的NaOH溶液,混合液pH=7
C.醋酸的电离程度增大,c(H+)亦增大
D.溶液中 ![]() 不变
不变
【答案】D
【解析】解:A.醋酸是弱电解质,加水稀释促进醋酸电离,导致溶液中导电粒子数目增大,故A错误;
B.室温下pH=3的醋酸浓度大于0.001mol/L,pH=11的氢氧化钠浓度为0.001mol/L,二者等体积混合后醋酸有剩余,醋酸电离程度大于醋酸根离子水解程度导致溶液呈酸性,pH<7,故B错误;
C.醋酸电离程度增大,溶液中c(H+)可能增大,也可能减小,如加入碱溶液促进醋酸电离但氢离子浓度减小,升高温度促进醋酸电离氢离子浓度增大,故C错误;
D.温度不变醋酸电离平衡常数不变、离子积常数不变,所以 ![]() =
= ![]() =
= ![]() 不变,故D正确;
不变,故D正确;
故选D.
A.醋酸是弱电解质,加水稀释促进醋酸电离;
B.室温下pH=3的醋酸浓度大于0.001mol/L,pH=11的氢氧化钠浓度为0.001mol/L,二者等体积混合后醋酸有剩余;
C.醋酸电离程度增大,溶液中c(H+)可能增大,也可能减小;
D. ![]() =
= ![]() =
= ![]() .
.


科目:高中化学 来源: 题型:
【题目】中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注.
(1)As的原子结构示意图为 ![]() ,则其在周期表中的位置是 .
,则其在周期表中的位置是 .
(2)N元素非金属性比As强,下列说法正确的是 . ①NH3的热稳定性比AsH3差
②HNO3的酸性比H3AsO4强
③N的原子半径比As的原子半径小
(3)根据如图写出As2O5分解为As2O3的热化学方程式 . 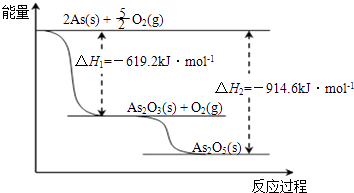
(4)查文献得知,可以从硫化砷(As2S3)废渣中提取As2O3 , 提取的工艺流程简图如下: 
①As2S3、Na3AsS3中的S均为﹣2价,碱浸过程中发生的反应(填“是”或“不是”)氧化还原反应.
②过程Ⅲ的系列操作包括 .
③写出过程Ⅲ的离子方程式 ,
过程Ⅲ中,酸性越强,As2O3的产率越高,请解释其原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于![]() Lv的叙述错误的是( )
Lv的叙述错误的是( )
A.原子序数116
B.中子数177
C.核外电子数116
D.相对原子质量293
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL 0.1 molL﹣1NaOH溶液中加入0.1molL﹣1的一元酸HA溶液pH的变化曲线如图所示.下列说法正确的是( ) 
A.a点所示溶液中c(Na+)>c(A﹣)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A﹣)+c(HA)
D.b点所示溶液中c(A﹣)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为反应:H2(g)+Cl2(g)=2HCl(g)的能量变化示意图,下列说法正确的是( ) 
A.该反应的反应热△H=﹣183kJmol﹣1
B.该反应生成液态HCl比生成气态HCl释放的能量少
C.氯气分子中的化学键比氢气分子中的化学键更稳定
D.1 mol HCl分子中的化学键形成时吸收431kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用软锰矿(主要含MnO2,还含有少了SiO2、Al2O3 、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。

(1)配平焙烧时MnO2参与的化学反应:□MnO2+□_____+□O2 ![]() □K2MnO4+□H2O;第二次通入过量CO2时发生反应的离子方程式为:______________________。
□K2MnO4+□H2O;第二次通入过量CO2时发生反应的离子方程式为:______________________。
(2)滤渣I、II的成分中能与NaOH 反应的是__________________ (填化学式)。产生滤渣II时不能用稀盐酸代替CO2,因为______________________。
(3)将滤液Ⅲ进行一系列操作可得到KMnO4晶体。由下图可知,从滤液Ⅲ得到KMnO4需经过____、____洗涤等操作。

(4)用重结晶提纯的产品配制成0.10mol·L-1 的酸性KMnO4溶液来测定某草酸样品的纯度(杂质不参与反应,草酸为弱酸,分子式H2C2O4)。
①试给出反应的离子方程式:_______________________。
②若某测定大致共需要230毫升酸性KMnO4溶液,配制时所需玻璃仪器为:___、___烧杯、胶头滴管等。
③取草酸样品5 克,配成100mL溶液,取20mL于适当容器中,用前述所配酸性KMnO4溶液滴定,至反应结束消耗KMnO4溶液20mL,则样品的纯度为: ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)氨碱法制纯碱包括石灰石分解、粗盐水精制、氨盐水碳酸化等基本步骤。
完成下列计算:
(1)CaCO3质量分数为0.90的石灰石100 kg完成分解产生CO2 L(标准状况)。石灰窑中,该石灰石100 kg与焦炭混合焙烧,产生CO2 29120 L(标准状况),如果石灰石中碳酸钙完全分解,且焦炭完全燃烧,不产生CO,则焦炭的物质的量为 mol。
(2)已知粗盐水含MgCl2 6.80 mol/m3 , 含CaCl2 3.00mol/m3。
向粗盐水中加入Ca(OH)2除镁离子:MgCl2 + Ca(OH)2 → Mg(OH)2↓ + CaCl2
然后加入Na2CO3除钙离子。处理上述粗盐水10 m3 , 至少需要加Na2CO3 g。
如果用碳酸化尾气(含NH3体积分数为0.100、CO2体积分数0.040)代替碳酸钠,发生如下反应: Ca2+ + 2NH3 + CO2 + H2O → CaCO3↓ + 2NH4+
处理上述10 m3粗盐水至少需要通入多少L(标准状况)碳酸化尾气?列式计算。
(3)某氨盐水含氯化钠1521 kg,通入二氧化碳后析出碳酸氢钠晶体,过滤后溶液中含氯化铵1070 kg。列式计算:
(1)过滤后溶液中氯化钠的质量。
(2)析出的碳酸氢钠晶体的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com