
【题目】在相同温度下,等体积等物质的量浓度的4种稀溶液:①Na2SO4、②H2SO4、③NaHSO4、④Na2S中所含离子种类由多到少的顺序是( )
A.①=④>③=②
B.④=①>③>②
C.①>④>③>②
D.④>①=③>②
【答案】D
【解析】解:①Na2SO4是强电解质,能在水溶液中完全电离:Na2SO4=2Na++SO ![]() ,且由于Na2SO4是强酸强碱盐,故不水解,故溶液中的离子有四种:Na+、SO
,且由于Na2SO4是强酸强碱盐,故不水解,故溶液中的离子有四种:Na+、SO ![]() 、H+、OH﹣; ②H2SO4是强酸,能在水溶液中完全电离:H2SO4=2H++SO
、H+、OH﹣; ②H2SO4是强酸,能在水溶液中完全电离:H2SO4=2H++SO ![]() ,故溶液中的离子种类有三种:H+、SO
,故溶液中的离子种类有三种:H+、SO ![]() 、OH﹣;
、OH﹣;
③NaHSO4是强电解质,能在水溶液中完全电离:NaHSO4=Na++SO ![]() +H+ , 且由于NaHSO4是强酸强碱盐,故不水解,故溶液中的离子有四种:Na+、SO
+H+ , 且由于NaHSO4是强酸强碱盐,故不水解,故溶液中的离子有四种:Na+、SO ![]() 、H+、OH﹣;
、H+、OH﹣;
④Na2S是强电解质,在溶液中完全电离:Na2S=2Na++S2﹣ , 但由于S2﹣是二元弱酸根,故在溶液中水解:S2﹣+H2OHS﹣+OH﹣ , HS﹣+H2OH2S+OH﹣ , 故溶液中的离子种类有五种:Na+、S2﹣、HS﹣、OH﹣、H+ .
故选D.


科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)COS(g)+H2(g) K=0.1
反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
A.升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】接触法制硫酸的核心反应是2SO2(g)+O2(g)2SO3(g)△H<0.
(1)该反应的平衡常数K值的表达式:K=;升高温度,K值将(填“增大”、“减小”、“不变”)
(2)生产中用过量的空气能使SO2的转化率(填“增大”、“减小”、“不变”)
(3)恒温恒容条件下,体系中充入氦气,化学反应速率(填“增大”、“减小”、“不变”)化学平衡(填“向右移动”、“向左移动”、“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:
a | |||||||||||||||||
b | d | e | |||||||||||||||
f | k | m | |||||||||||||||
n | p | ||||||||||||||||
(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界__________;
(2)表中最活泼的金属与最活泼的非金属形成的物质是_____________(填化学式);
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:__________,这两种化合物中所含的化学键有________(填序号);
A.极性共价键 B.非极性共价键 C.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为___________(填离子符号);
(5)d、m对应的离子还原性由强到弱顺序为__________________(填离子符号);
(6)d、e、m、p的气态氢化物中,最不稳定是___________(填分子式);
(7)用电子式表示n与m形成的原子个数比2:1的化合物的形成过程___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH﹣△H>0,下列叙述正确的是( )
A.向水中加入氨水,平衡逆向移动,c(OH﹣)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置图的叙述中,正确的是( ) 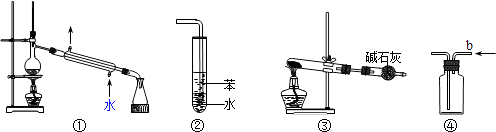
A.装置①可用于分离苯和溴苯的混合物
B.装置②可用于吸收HCl或NH3气体
C.装置③可用于分解NH4Cl制备NH3
D.装置④b口进气可收集CO2或NO气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品﹣3PbOPbSO4H2O (三盐),主要制备流程如下:
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为 .
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为(写化学式).
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为;滤液2中溶质主要成分为(写化学式).
(4)步骤⑥合成三盐的化学方程式为 .
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,细菌GFAJ-1能利用化学元素砷(As)取代磷(P)参与化合物组成。下列相关叙述正确的是( )
A.该细菌的组成元素砷(As)可能在无机自然界中找不到
B.As在该细菌体内的含量高于氧元素
C.该细菌通过分裂产生子代
D.该细菌的拟核区含有一个裸露的链状DNA分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com