
【题目】某溶液中可能存在Mg2+、Fe2+、Fe3+ , 加入NaOH溶液,开始时有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( ) 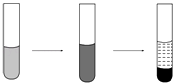
A.一定有Fe2+ , 一定没有Fe3+、Mg2+
B.一定有Fe3+ , 一定没有Fe2+、Mg2+
C.一定有Fe3+ , 可能有Fe2+ , 一定没有Mg2+
D.一定有Fe2+ , 可能有Mg2+ , 一定没有Fe3+
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识填写下列空白.
(1)有机物 ![]() 的系统名称是 , 将其在催化剂存在下完全氢化,所得烷烃的系统名称是 . 该烷烃的一氯代物最多有种.
的系统名称是 , 将其在催化剂存在下完全氢化,所得烷烃的系统名称是 . 该烷烃的一氯代物最多有种.
(2)2,3﹣二甲基﹣4﹣乙基已烷结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下N2+3H2=2NH3为放热反应,下列说法正确的是( )
A.该反应是可逆反应
B.反应达到平衡时,反应速率为零
C.氢气可以完全转化为氨气
D.反应物的总能量小于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里有4个药品橱,已经存放以下物品:
药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 盐酸,硫酸 | 氢氧化钠,氢氧化钙 | 红磷,硫 | 铜,锌 |
实验室新购进一些碘,应该将这些碘放在( )
A.甲橱B.乙橱C.丙橱D.丁橱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,某学习小组为了探究二氧化硫的某些性质,进行了如下实验。
I.如下图所示,使用药品和装置一探究二氧化硫的还原性:
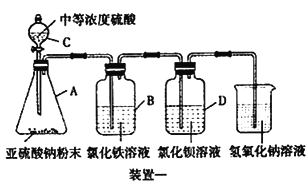
(1)装置C的名称为________。
(2)B中溶液的现象为________。
(3)学生甲预测装置D 中没有白色沉淀产生,但随着反应的进行,发现D 中产生了少量白色沉淀。学生乙经过查阅资料发现少量白色沉淀可能是硫酸钡,因为装置或溶液中少量的氧气参与了氧化反应,请写出装置D 中的反应方程式________。
II.经过思考,设计了如下装置二,且所配制的溶液均使用无氧蒸馏水,检验SO2 在无氧干扰时,是否与氯化钡反应生成沉淀。
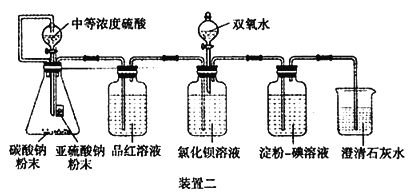
(4)碳酸钠粉末的目的是________。
(5)当______时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(6)裝置二选用澄清石灰水而不用氢氧化钠溶液的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对乙烯基苯甲酸是重要的医药中间体,广泛应用于合成感光材料。对乙烯基苯甲酸可通过如下反应合成。
反应①: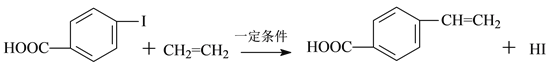
I II
(1)下列关于化合物I和化合物II的说法,正确的是______。
A.化合物I能与新制的Cu(OH)2反应
B.均可发生酯化反应和银镜反应
C.化合物II能使KMnO4溶液褪色
D.1mol化合物II最多能与5 mol H2反应
(2)化合物II的分子式为____________,化合物II在催化剂条件下生产高分子化合物的反应方程式___________________________________________________________。
(3)化合物II可由芳香族化合物Ⅲ通过消去反应获得,Ⅲ和Cu共热的产物能发生银镜反应,写出化合物Ⅲ的结构简式_______________________;
(4)化合物IV是化合物II的同分异构体,且化合物IV遇FeCl3溶液显紫色,苯环上的一氯代物只有2种,写出化合物IV的结构简式____________________________(写一种)。
(5)利用类似反应①的方法,仅以溴苯(![]() )和乳酸(
)和乳酸(![]() )为有机物原料合成化工原料肉桂酸(
)为有机物原料合成化工原料肉桂酸(![]() ),涉及的反应方程式为________________________________;___________________________________。
),涉及的反应方程式为________________________________;___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3和NaHCO3的性质说法正确的是
A. 溶解度:Na2CO3>NaHCO3
B. 右图所示装置可证明稳定性:Na2CO3>NaHCO3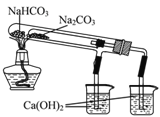
C. 用澄清石灰水可鉴别Na2CO3溶液和NaHCO3溶液
D. 等质量的Na2CO3和NaHCO3分别与过量盐酸反应,放CO2质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液是一种以NaClO为主的消毒剂,广泛应用于医院、食品加工、家庭等的卫生消毒。
(1)“84”消毒液中通入CO2能增强消毒效果,写出向“84”消毒液中通入过量CO2的离子方程式:___________________。
(2)测定“84”消毒液中NaClO的物质的量浓度的方法如下:
①配制100.00mL 0.5000 mol·L-1的Na2S2O3溶液。配制过程中需准确称取Na2S2O3固体___________________g,需要用到的玻璃仪器有烧杯、胶头滴管、量筒、___________________。
②准确量取10.00 mL消毒液于锥形瓶中,加入过量的KI溶液,用足量的乙酸酸化,充分反应后向溶液中滴加Na2S2O3溶液,完全反应时消耗Na2S2O3溶液25.00 mL。反应过程中的相关离子方程式为:
2CH3COOH+2I—+ClO—=I2+Cl—+2CH3COO—+H2O,I2+2S2O![]() =2I—+S4O
=2I—+S4O![]()
通过计算求出该“84”消毒液中NaClO的物质的量浓度。(写出计算过程)__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mo1/LHCl溶液滴定10.mL0.1mol·L-1Na2CO3溶液,滴定曲线如图所示。下列说法正确的是( )
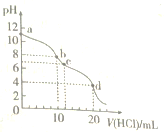
A. 水电离程度由大到小的顺序为:a>b>c>d
B. a点时:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
C. b点时:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D. d点时:c(H+)>c(HCO3-)=c(CO32-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com