
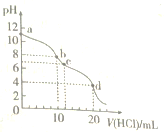
【题目】室温下,用0.1mo1/LHCl溶液滴定10.mL0.1mol·L-1Na2CO3溶液,滴定曲线如图所示。下列说法正确的是( )
A. 水电离程度由大到小的顺序为:a>b>c>d
B. a点时:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
C. b点时:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D. d点时:c(H+)>c(HCO3-)=c(CO32-)
【答案】A
【解析】b点10mL 0.1mo1/L HCl溶液与10 mL0.1mol/LNa2CO3溶液混合,恰好反应为NaHCO3与NaCl,即b点溶质为NaHCO3与NaCl;d点20mL 0.1mo1/L HCl溶液与10 mL0.1mol/LNa2CO3溶液混合,恰好完全反应生成NaCl与CO2,而d点溶液呈酸性,则溶解了CO2,溶质为NaCl与H2CO3;c点存在NaHCO3、NaCl,而pH=7,则溶液中也存在H2CO3。综上分析,a点溶质为Na2CO3;b点溶质为NaHCO3、NaCl;c点溶质为NaHCO3、H2CO3、NaCl;d点溶质为NaCl、H2CO3;
A、a、b点均促进水的电离,且对水电离的促进作用a>b,c点pH=7,NaHCO3促进水的电离,H2CO3抑制水的电离,两者作用相互抵消,d点抑制水的电离,故水电离程度大小顺序为a>b>c>d,故A正确。B、a点溶质为Na2CO3,CO32-部分水解生成HCO3-和OH-,溶液呈碱性,由于OH-还来自水的电离,则c(OH-)>c(HCO3-),离子浓度大小为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-),故B错误;C、b点溶质为NaHCO3、NaCl,根据物料守恒:c(Na+)= 2[c(CO32-)+c(HCO3-)+c(H2CO3)],故C错误;D、d点溶质为NaCl、H2CO3;H2CO3以第一步电离为主,则c(HCO3-)<c(CO32-),由于H+还来自水的电离,则c(HCO3-)>c(H+),正确的离子浓度大小为:c(H+)>c(HCO3-)>c(CO32-),故D错误;故选A。


科目:高中化学 来源: 题型:
【题目】某溶液中可能存在Mg2+、Fe2+、Fe3+ , 加入NaOH溶液,开始时有白色絮状沉淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( ) 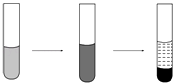
A.一定有Fe2+ , 一定没有Fe3+、Mg2+
B.一定有Fe3+ , 一定没有Fe2+、Mg2+
C.一定有Fe3+ , 可能有Fe2+ , 一定没有Mg2+
D.一定有Fe2+ , 可能有Mg2+ , 一定没有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.活化分子间的碰撞一定是有效碰撞
B.活化分子具有的能量是活化能
C.活化分子的总数越多,反应速率越快
D.单位时间内有效碰撞次数越多,反应速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A.糖类、油脂、蛋白质都是高分子化合物
B.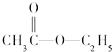 与 H
与 H ![]() O发生水解反应,生成的产物中18O存在于乙醇中
O发生水解反应,生成的产物中18O存在于乙醇中
C.除去乙酸乙酯中混有的乙酸,可以加入乙醇继续酯化
D.油脂不管在哪种条件下水解都生成丙三醇(甘油)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用药品羟苯水杨胺,其合成路线如图.回答下列问题: 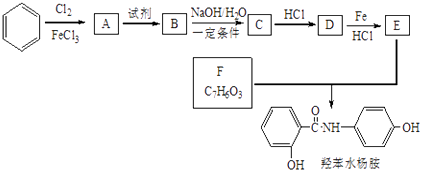
已知: 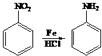
(1)羟苯水杨胺的分子式为 . 对于羟苯水杨胺,下列说法正确的是(填序号).
a.1mol羟苯水杨胺最多可以和2mol NaOH反应
b.不能发生硝化反应
c.可发生水解反应
d.可与溴发生取代反应
(2)D的名称为 .
(3)A→B所需试剂为;D→E反应的有机反应类型是 .
(4)B→C反应的化学方程式为 .
(5)写出 F的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应的,且其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:2:1的同分异构体的一种结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某火力发电厂以煤为燃料,排出的废气中含有CO2、SO2、水蒸气。为检验该废气中的成分,用如图所示的装置进行实验:

(1)仪器连接的顺序为(填导管接口字母) ;
(2)根据 现象证明有CO2;
(3)装置B的作用是 ,装置D的作用是 。
II. 为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)

(4)亚硫酸钠与浓硫酸反应的化学方程式: ;
(5)为探究干燥的SO2 能不能使品红褪色,请指出设计的实验装置图中两个明显的不足:
① ,
② ;
(6)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。这说明品红褪色的原因不是SO2直接导致。所以,SO2 通过品红水溶液后,引起品红褪色的微粒可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子:化合物B2E的晶体为离子晶体,E原子核外的M层中有两对成对电子:C元素是底壳中含量最高的金属元素:D单质的熔点在同周期元素形成的单质中是最高的:F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为______(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是______。
(3)E的最高价氧化物分子的空间构型是______。是______分子(填“极性”“非极性”)
(4)F原子的价层电子排布式是_____。
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子)。其化学式为_____。(a)中E原子的配位数为______,若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有_____个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)________(b)(填“>”“<”或“=”)
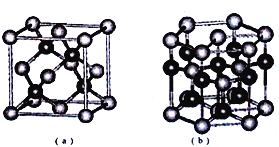
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CeO2是一种重要的稀土氧化物,可利用氟碳铈矿(主要成分为CeFCO3)来制备。其工艺流程如下:

已知:I.Ce4+能与SO42-结合成[CeSO4]2+,与F-结合成[CeFx](4-x)+(0<x<4).
II.在硫酸体系中,Ce4+能被萃取剂萃取二Ce3+不能。
回答下列问题:
(1)“氧化焙烧”中“氧化”的目的是_________________。
(2)CeO2不溶于水和碱,微溶于酸,但“浸出”时却能溶解完全,原因是溶液中的_______(填原子符号,下同)、__________、_____________促进了CeO2的溶解。
(3)“反萃取”时发生反应的离子方程式为____________________。
(4)若缺少“洗氟”这一环节,则所得产品的质量将___________(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com