
【题目】如图所示为CH4燃料电池的装置(A、B为多孔碳棒):

(1)_____(填A或B)处电极入口通甲烷,其电极反应式为_____________;
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,消耗KOH的质量为_______g。
(3)铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极的电极反应为____________________。
(4)500 mL KNO3和Cu(N03)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL。原混合溶液中c(K+)为_________mol·L-1。
【答案】 B CH4+10OH--8e-===CO32-+7H2O 56 PbO2+2e-+SO42-+4H+=PbSO4+2H2O 2
【解析】(1)根据电子的移动方向是有负极→外电路→正极,甲烷应通入B极,甲烷跟氧气在碱性溶液中反应生成碳酸根离子,电极反应式为CH4+10OH--8e-===CO32-+7H2O;(2)总方程式为:CH4+2O2+2OH—=CO32—+3H2O,当消耗甲烷的体积为11.2 L(标准状况下)时,根据电极方程式知,消耗KOH的质量为0.5mol![]() 6g/mol=56g;(3)铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极PbO2得电子生成硫酸铅,其电极反应为:PbO2+2e-+SO42-+4H+=PbSO4+2H2O;(4)石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),n(O2)=
6g/mol=56g;(3)铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极PbO2得电子生成硫酸铅,其电极反应为:PbO2+2e-+SO42-+4H+=PbSO4+2H2O;(4)石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),n(O2)=![]() =1mol,
=1mol,
阳极发生4OH--4e-═O2↑+2H2O,
4mol 1mol
阴极发生Cu2++2e-═Cu、 2H++2e-═H2↑,
1mol 2mol 1mol 2mol 1mol
c(Cu2+)=![]() =2mol/L,由电荷守恒可知,原混合溶液中c(K+)为6mol/L-2mol/L×2=2mol/L。
=2mol/L,由电荷守恒可知,原混合溶液中c(K+)为6mol/L-2mol/L×2=2mol/L。


科目:高中化学 来源: 题型:
【题目】已知N2+3H2 ![]() 2NH3为放热反应,对该反应的下列说法中正确的是 ( )
2NH3为放热反应,对该反应的下列说法中正确的是 ( )
A. N2的能量一定高于NH3
B. H2的能量一定高于NH3
C. 1 mol N2和3 mol H2的总能量一定高于2 mol NH3的总能量
D. 因该反应为放热反应,故不必加热就可发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施不影响食品安全的是( )
A. 用乙烯催熟果实B. 用聚氯乙烯薄膜包装食品
C. 往珍珠奶茶的珍珠中添加塑化剂D. 用福尔马林作食品防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学在完成课本乙醇制乙醛的实验后,改进了实验方案(如图)按下列顺序进行如下实验操作。
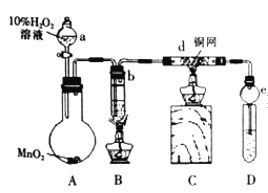
①连接好仪器,检验装置的气密性;
②正确添加试剂;
③点燃C装置中的酒精灯;
④向圆底烧瓶中滴加10%过氧化氢溶液;
⑤点燃B装置中的酒精灯加热无水乙醇至沸腾并持续加热。
根据以上所有内容回答下列问题:
(1)装置e的作用是______________;
(2)写出d中发生反应的化学方程式__________________________;
(3)为检验D中收集的产物中是否含有乙醛,甲同学利用银氨溶液检验,请写出化学反应方程式_______________________;
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如下表):
实验变量 实验序号 | 银氨溶液的S/mL | 乙醛的量/滴 | 温度/℃ | 反应混合液的pH值 | 出现银镜的时间/min |
1 | 1 | 3 | 65 | 11 | 5 |
2 | 1 | 3 | 45 | 11 | 6.5 |
3 | 1 | 5 | 65 | 11 | 4 |
①实验1和实验2,探究的实验目的是_________________________。
②当银氨溶液的量为lmL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为_________min。(填范围)
(5)若试管中收集到的液体用紫色石蕊试液检验,溶液显红色,说明液体中还含有___________(填物质名称),要除去该物质,可先在混合液中加入_________(填写下列选项中的字母),然后再通过___________(填操作名称)即可除去。
A.饱和NaCl溶液 B.C2H5OH C.NaHCO3溶液 D.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_____________(填“氧化性”或“还原性”),Fe3+有_____________(填“氧化性”或“还原性”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③单质溴和氯化钠的水溶液,分离以上各混合液的正确方法依次是 ( )
A. 分液、萃取、蒸馏B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸(HOOC—COOH)也称草酸,是一种重要的化工原料和化工产品。利用石油化工产品中的烷烃可以生成草酸,生产流程如下:
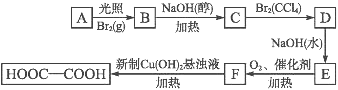
已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79。
请回答下列问题:
(1)A的结构简式是_______________;D的名称__________________。
(2)写出有关的化学方程式:
B→C:________________________________________________________。
D→E:________________________________________________________。
(3)A生成B的反应类型是__________;C生成D的反应类型是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族有机物的分子式为C11H14O2,能与NaOH溶液反应,苯环上只有两个取代基,其中有一个是-C4H9,满足条件的该有机物有
A. 6种 B. 12种 C. 18种 D. 24种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述正确的是( )
A. 新制氯水中只有Cl2分子和H2O分子
B. 光照氯水有气体逸出,该气体是Cl2
C. 氯水在密闭无色玻璃瓶中放置数天后酸性将减弱
D. 新制氯水可以使蓝色石蕊试纸先变红后褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com