
1-36号A、B、C、D、E 、F六种元素,其中A、B、C、D、E的原子序数均小于18且其核电荷数依次递增,B元素基态原子电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,D原子的价电子排布为ns2np2n+2, E原子第一至第四电离能(kJ·mol-1)分别为:738、1451、7733、10540。F2+离子K、L、M层全充满。根据以上信息,同答下列问题:
(1)BA4D和BA2D,沸点较高的是 (填相关物质的结构简式)
(2)已知B与A形成的化合物在标准状况下的密度为1.16g·L-1,则在该化合物分子空间构型 ,在该化合物分子中含有σ键和π键个数比 。
(3)写出单质F与足量C的最高价氧化物对应的水化物稀溶液反应,C被还原到最低价,该反应的化学方程式 。
(4)下图能正确表示第三周期部分元素的第二电离能(I2)与原子序数关系 (填标号)。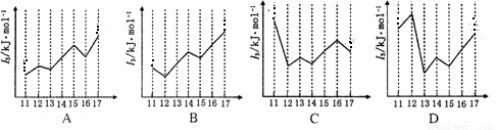
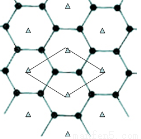
(5)B的单质是一种层状结构,元素B和E的形成一种合金,E的原子位于B的层间,其投影位于层面六圆环的中央,“△”表示E的原子位置,平行四边形表示在此二维图形上画出的一个晶胞,该合金的化学式为________。
(1)CH3OH;(2)直线;3::2;(3)4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O; (4)C; (5)MgC2。
【解析】
试题分析:根据题意可知A是H;B是C;C是N;D是O;E是Mg;F是Zn。(1)BA4D是CH3OH,BA2D是HCHO,二者的分子之间都存在氢键,由于甲醇的相对分子质量比甲醛的大,所以分子之间的吸引力甲醇的大,因此沸点较高的是CH3OH;(2)已知B与A形成的化合物在标准状况下的密度为1.16g·L-1,则该分子的相对分子质量是:1.16×22.4=26,该分子是CH≡CH,所以在该化合物分子空间构型直线型;在该化合物分子中含有σ键和π键个数比3:2;(3)单质Zn与足量C的最高价氧化物对应的水化物HNO3稀溶液反应,C被还原到最低价,该反应的化学方程式s是4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O;(4)当原子核外的电子处于该轨道的半充满、全充满时是稳定的状态,失去电子较难,所以能正确表示第三周期部分元素的第二电离能(I2)与原子序数关系是C;(5)在每一个晶胞中含有Mg:1;含有C:6×1/3=2,所以化学式是MgC2。
考点:考查元素的推断、元素形成的化合物的结构、性质及化学式的确定的知识。


科目:高中化学 来源:2013-2014辽宁省高三仿真测试理科综合化学试卷(解析版) 题型:填空题
海洋是一个丰富的资宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和 池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用: (写一点即可)。
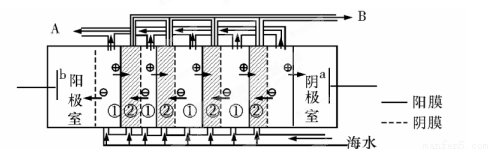
(2)电渗析法是近年发展起的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
①海水不能直接通入到阴极室中,理由是 。
②A口排出的是 (填“淡水”或“浓水”)。
(3)用苦卤(含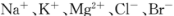 等离子)可提取溴,其生产流程如下:
等离子)可提取溴,其生产流程如下:

①若吸收塔中的溶液含BrO3-,则吸收塔中反应的离子方程式为: 。
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化重新获得含Br2的溶液? 。
③向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建龙岩市毕业联合考试理综化学试卷(解析版) 题型:选择题
对于反应aA+bB=dD+eE,该化学反应速率定义为 。式中
。式中 指物质
指物质 的反应速率,
的反应速率, 、
、 、
、 、
、 是化学计量数。298k时,测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时化学反应速率v见下表:
是化学计量数。298k时,测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时化学反应速率v见下表:
实验编号 | 1 | 2 | 3 | 4 |
c(HI)/ mol·L-1 | 0.100 | 0.200 | 0.300 | 0.100 |
c(H2O2)/ mol·L-1 | 0.100 | 0.100 | 0.100 | 0.200 |
v/ mol·L-1·s-1 | 0.00760 | 0.0153 | 0.0227 | 0.0151 |
以下说法正确的是
A.实验1、2中, (H2O2)相等
(H2O2)相等
B.将浓度均为0.200 mol·L-1H2O2和HI溶液等体积混合,反应开始时 =0.0304 mol·L-1·s-1
=0.0304 mol·L-1·s-1
C. 与“HI和H2O2浓度的乘积”的比值为常数
与“HI和H2O2浓度的乘积”的比值为常数
D.实验4,反应5秒后H2O2浓度减少了0.0755 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:推断题
(13分)(1).PET是应用广泛的五大工程塑料之一,PET结构片段:
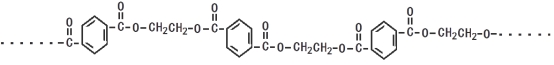
①PET由两种有机物通过缩聚反应生成,其中分子较大的单体分子结构简式为 ,分子较小的单体含氧官能团名称是 。
②PET塑料有多种降解途径,其中常用的甲醇法是在一定条件下将其与过量的甲醇作用,降解为两种小分子。该反应的化学方程式为: 。
(2).水杨酸(邻羟基苯甲酸)是合成阿司匹林(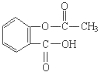 )的原料。
)的原料。
①水杨酸与乙酸酐(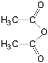 )反应生成阿司匹林的化学方程式: 。
)反应生成阿司匹林的化学方程式: 。
②写出一种阿司匹林同分异构体的结构式 ,该同分异构体符合以下条件:
a.芳香族化合物;
b.与氢氧化钠溶液共热,完全反应将消耗四倍物质的量的氢氧化钠;
c.苯环上氢原子被一个溴原子取代,可能的产物有两种。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),下列说法正确的是 ( )
2Z(g),下列说法正确的是 ( )
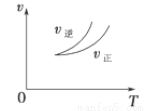
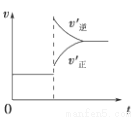
A.左上图说明正反应为吸热反应
B.反应达平衡后,增大压强气体密度将减小
C.右上图可表示升高温度使平衡向逆反应方向移动
D.右上图虚线可表示使用催化剂后引发的反应速率变化
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
短周期元素X、Y、W、Q在元素周期表中的相对位置如下图所示。Y是地壳中含量最多的元素。下列说法正确的是( )
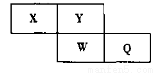
A.1mol Q单质与氢氧化钠溶液反应转移的电子数目为2 NA
B.X的气态氢化物能使湿润的蓝色石蕊试纸变红
C.氢化物的沸点:H2Y>HQ
D.最髙价氧化物的水化物的酸性:W > Q
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
下列数据是对应物质的熔点,有关的判断错误的是( )
Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
920℃ | 97.8℃ | 1291℃ | 190℃ | 2073℃ | -107℃ | -57℃ | 1723℃ |
A.含有金属阳离子的晶体不一定是离子晶体
B.在共价化合物分子中各原子都形成8电子结构
C.同族元素的氧化物可形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:填空题
短周期元素X、Y、Z、W 的原子序数依次增大, X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素.X、Y、Z、W 原子最外层电子数之和为13。问:
(1)X是 Y是 Z是 W是 (填元素符号)
(2)写出W的最高价氧化物对应的水化物的电子式
写出Y的简单氢化物的电子式
(3)Y的最高价氧化物对应的水化物的浓溶液久置后呈现黄色,写出发生反应的化学方程式
(4)实验室制取Y的氢化物的化学方程式:_______________________________,该反应________(填“是”或“不是”)氧化还原反应。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:实验题
(15分)实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
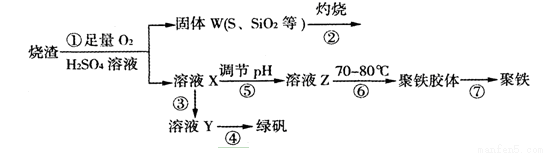
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是 ;
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为: ;
(3)过程③中,需加入的物质是 ;
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有 ;
(5)过程⑤调节pH可选用下列试剂中的 (填选项序号);
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70一80℃,目的是 ;
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.700g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为[(Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为 。(假设杂质中不含铁元素和硫元素)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com