
短周期元素X、Y、W、Q在元素周期表中的相对位置如下图所示。Y是地壳中含量最多的元素。下列说法正确的是( )
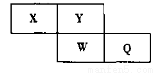
A.1mol Q单质与氢氧化钠溶液反应转移的电子数目为2 NA
B.X的气态氢化物能使湿润的蓝色石蕊试纸变红
C.氢化物的沸点:H2Y>HQ
D.最髙价氧化物的水化物的酸性:W > Q
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014辽宁省高三仿真测试理科综合化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | R | Q | |
原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | —— |
最低负价 | —— | -1 | —— | ——- | -3 | -2 | |
下列说法正确的是
A.元素X和Q形成的化合物中不可能含有共价键
B.X、Y、M的单质分别与水反应,Y最剧烈
C.X、Z、R的最高价氧化物的水化物之间可两两相互反应
D.Y的氧化物水化物的酸性一定强于R的的氧化物水化物的酸性
查看答案和解析>>
科目:高中化学 来源:2013-2014福建龙岩市毕业联合考试理综化学试卷(解析版) 题型:选择题
下列与有机物的结构、性质有关的叙述正确的是
A.用新制氢氧化铜悬浊液无法鉴别葡萄糖和乙酸
B.乙酸与乙醇可以发生酯化反应,又均可与碳酸氢钠溶液反应
C.硫酸铵、硫酸铜和乙醇均能使蛋白质变性
D.二氯甲烷不存在同分异构体
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
常温下,向l00mL 0.01 mol?L-1 盐酸中逐滴加入0.02 mol?L-1 MOH溶液,如下图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是( )
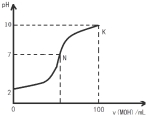
A.MOH是弱碱
B.N点c(Cl-) = c(M+)
C.随着MOH溶液的滴加,比值 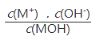 不变
不变
D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol?L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:填空题
1-36号A、B、C、D、E 、F六种元素,其中A、B、C、D、E的原子序数均小于18且其核电荷数依次递增,B元素基态原子电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,D原子的价电子排布为ns2np2n+2, E原子第一至第四电离能(kJ·mol-1)分别为:738、1451、7733、10540。F2+离子K、L、M层全充满。根据以上信息,同答下列问题:
(1)BA4D和BA2D,沸点较高的是 (填相关物质的结构简式)
(2)已知B与A形成的化合物在标准状况下的密度为1.16g·L-1,则在该化合物分子空间构型 ,在该化合物分子中含有σ键和π键个数比 。
(3)写出单质F与足量C的最高价氧化物对应的水化物稀溶液反应,C被还原到最低价,该反应的化学方程式 。
(4)下图能正确表示第三周期部分元素的第二电离能(I2)与原子序数关系 (填标号)。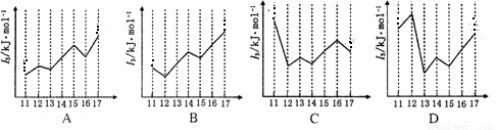
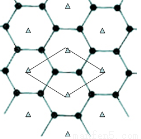
(5)B的单质是一种层状结构,元素B和E的形成一种合金,E的原子位于B的层间,其投影位于层面六圆环的中央,“△”表示E的原子位置,平行四边形表示在此二维图形上画出的一个晶胞,该合金的化学式为________。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
下列变化或数据与氢键无关的是( )
A.甲酸蒸气的密度在373K时为1.335g·L-1,在293K时为2.5 g·L-1
B.氨分子与水分子形成一水合氨
C.水结冰体积增大。
D.SbH3的沸点比PH3高
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是
A | B |
C |
|
①B、C形成的单质均存在同素异形体 ②X的种类比Y多
③常温下,B的氢化物不能电离出H+ ④C的最高价氧化物对应的水化物是强酸( )
A.①②③④ B.②④ C.①② D.①③
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
已知破坏1 mol H—H键、Cl—Cl键、H—Cl键分别需要吸收436 kJ、243 kJ、432 kJ能量,则由H2与Cl2生成1 mol HCl总的过程需要( )
A.放热185 kJ B.吸热185 kJ C.放热92.5 kJ D.吸热92.5 kJ
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:选择题
下列选项合理的是( )
A.pH皆等于3 的两种溶液都稀释100倍后,pH都为5
B.10mL 0.02mol/L HCl溶液与10mL 0.02mol/L Ba(OH) 2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7
C.在0.1mol/L某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
D.室温下,在一定量稀氨水中逐滴滴入稀盐酸,对于所得溶液中离子浓度大小关系
可能是:c(NH4+)>c(Cl—)>c(OH—)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com