
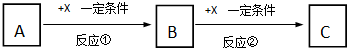
���� ��1��X��ǿ���������嵥�ʣ������뵽X��O2��ʵ��ת����ϵ��ABC�к���ͬԪ���Ҵ��ڱ�ۣ���ʵ��ͼʾת����ϵ�Ŀ���ΪC��CO��CO2��Na��Na2O��Na2O2��
��2����X�ǽ������ʣ���C��ˮ��Һ�еμ�AgNO3��Һ������������ϡHNO3�İ�ɫ������X��A��ȼ�ղ����ػ�ɫ���̣���֪XΪFe��A��B��C�ֱ�ΪCl2��FeCl3��FeCl2��
��3����XΪǿ��ʱ����ʵ��ͼʾת����ϵΪAlCl3��Al��OH��3��NaAlO2����XΪǿ��ʱ����ʵ��ͼʾת����ϵΪNaAlO2��Al��OH��3��AlCl3�����BΪAl��OH��3��
��� �⣺��1��X��ǿ���������嵥�ʣ������뵽X��O2��ʵ��ת����ϵ��ABC�к���ͬԪ���Ҵ��ڱ�ۣ���ʵ��ͼʾת����ϵ�Ŀ���ΪC��CO��CO2��Na��Na2O��Na2O2��
�ʴ�Ϊ��ac��
��2����X�ǽ������ʣ���C��ˮ��Һ�еμ�AgNO3��Һ������������ϡHNO3�İ�ɫ������X��A��ȼ�ղ����ػ�ɫ���̣���֪XΪFe��A��B��C�ֱ�ΪCl2��FeCl3��FeCl2��
�����Ȼ�������������Fe����Ϊ��2Fe3++Fe=3Fe2+����ֹFe2+��������Fe3+��
�Ȼ�������Һ�м�NaOH����Ӧ�����������������������Ϊ�����������۲쵽������ɫ������Ѹ�ٱ�ɻ���ɫ�����ձ�Ϊ���ɫ�������漰��������ԭ��ӦΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��FeCl3��2Fe3++Fe=3Fe2+����ֹFe2+��������Fe3+��������ɫ������Ѹ�ٱ�ɻ���ɫ�����ձ�Ϊ���ɫ������4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��3����XΪǿ��ʱ����ʵ��ͼʾת����ϵΪAlCl3��Al��OH��3��NaAlO2����XΪǿ��ʱ����ʵ��ͼʾת����ϵΪNaAlO2��Al��OH��3��AlCl3�����BΪAl��OH��3����Ӧ�ڵ����ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��Al��OH��3+3H+=Al3++3H2O��
�ʴ�Ϊ��Al��OH��3��Al��OH��3+OH-=AlO2-+2H2O��Al��OH��3+3H+=Al3++3H2O��
���� ���⿼��������ƶϣ�������Ԫ�ػ�����֪ʶ���飬�������ʵ������ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
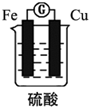
| A�� | �õ�ع���ʱ����ת��Ϊ��ѧ�� | B�� | ��Ƭ���������� | ||
| C�� | ͭƬ�Ϸ����ķ�Ӧ2H++2e-=H2�� | D�� | SO42-����Ƭ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ����ͭ�еμ�����Ũ���ᣬ������ɫ������ף�˵��Ũ���������ˮ�� | |
| B�� | ��δ֪��Һ�еμ�BaCl2��Һ�ð�ɫ������ȡ�ð�ɫ������ϡ����ܽ⣬˵��ԭδ֪��Һ�к���SO42- | |
| C�� | ��ͭƬ�ϵμ�����ϡ���ᣬ����������˵��ϡ����û�������� | |
| D�� | ijδ֪����ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ����ԭ����һ���� SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�ش��� | A | B | D | E | G | H | I | J |
| ���ϼ� | -1 | -2 | +4��-4 | +4��-2 | +5��-3 | +3 | +2 | +1 |
| ԭ�Ӱ뾶/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
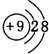 ��
��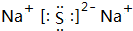 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 5�� | C�� | 4�� | D�� | 3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ����1��˫����ֱ���л��� | B�� | ����2��˫����ֱ���л��� | ||
| C�� | ����1��˫���Ļ�״�л��� | D�� | ����1��������ֱ���л��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��ˮ��Ӧ Na+2H2O�TNa++2OH-+H2�� | |
| B�� | ��AlCl3��Һ�м��������NaOH��Һ Al3++3OH-�TAl��OH��3�� | |
| C�� | ����������Һ��������Һ��Ӧ Ba2++OH-+H++SO42-�TBaSO4��+H2O | |
| D�� | CO2ͨ���������ʯ��ˮ CO2+Ca2++2OH-�TCaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
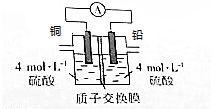 Ǧ��һ�ֻ��ý�����Ǧ��ϡ���ᷢ���ķ�ӦΪPb+H2SO4��aq���TPbSO4��s��+H2����ijͬѧ���ݷ�Ӧ�������װ�ã��ش��������⣺
Ǧ��һ�ֻ��ý�����Ǧ��ϡ���ᷢ���ķ�ӦΪPb+H2SO4��aq���TPbSO4��s��+H2����ijͬѧ���ݷ�Ӧ�������װ�ã��ش��������⣺�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com