
 某同学按如图所示的装置进行电解实验.下列说法正确的是( )
某同学按如图所示的装置进行电解实验.下列说法正确的是( )| A、电解过程中,铜电极上有H2产生 | ||||
| B、电解一定时间后,石墨电极不可能有铜析出 | ||||
C、电解初期,主反应方程式为:Cu+H2SO4
| ||||
| D、整个电解过程中,H+的浓度不断增大 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、变化时有电子的得失或共用电子对的形成 |
| B、变化过程中有旧化学键的断裂和新化学键形成 |
| C、变化前后原子的种类和数目没有改变,分子种类增加了 |
| D、变化时释放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体中一定有甲烷 |
| B、混合气体中一定是甲烷和乙烯 |
| C、混合气体中一定没有乙烷 |
| D、混合气体中可能有乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
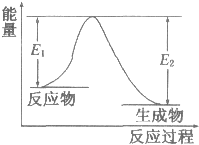
| A、该反应的△H<0 |
| B、反应体系中加入催化剂,E1减小,E2增大 |
| C、反应体系中加入催化剂,△H不变 |
| D、反应达到平衡时,升高温度,A的转化率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的密度不随时间变化而变化 |
| B、3v正(B)=v逆(D) |
| C、混合气体的压强保持不变 |
| D、B、C、D的分子数之比为3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的体积保持不变 |
| B、混合气体的密度保持不变 |
| C、混合气体平均相对分子质量保持不变 |
| D、混合气体颜色保持不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com