
| A. | FeO | B. | Fe2O3 | C. | FeSO4 | D. | Fe3O4 |
分析 假设质量都为mg,根据n=$\frac{m}{M}$计算各物质的物质的量,由电子转移守恒可知,失去电子物质的量越大生成NO越多.
解答 解:假设质量都为mg,
A.mgFeO与硝酸反应被氧化生成Fe3+,则失电子物质的量为$\frac{mg}{72g/mol}$×(3-2)=$\frac{m}{72}$mol;
B.Fe2O3与硝酸不发生氧化还原反应,失电子为0;
C.FeSO4与硝酸反应被氧化生成Fe3+,则失电子物质的量为$\frac{m}{152}$mol;
D.Fe3O4中Fe元素的化合价有+2、+3价,与硝酸反应被氧化生成Fe3+,则失电子物质的量为$\frac{mg}{232/mol}$×(9-3×$\frac{8}{3}$)=$\frac{m}{232}$mol,
由以上分析可知,失电子最多的是FeO,则放出NO物质的量最多的是FeO,
故选B.
点评 本题考查氧化还原反应的相关计算,注意把握Fe元素的化合价的变化,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硝酸、浓硫酸共热并保持50~60℃反应生成硝基苯 | |
| B. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于苯环对侧链的影响,使侧链易被氧化 | |
| C. | 若甲苯苯环上的一个氢原子被一个含3个碳原子的烷基取代,所得产物有6种 | |
| D. | 菲的结构简式为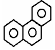 ,它与硝酸反应,可生成3种一硝基取代物 ,它与硝酸反应,可生成3种一硝基取代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 反应时间t/min | 0 | 1 | 2 | 3 | 4 |
| c(X)/(mol•L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属单质在化学反应中只能做还原剂 | |
| B. | 非金属单质在化学反应中只能做氧化剂 | |
| C. | 金属原子在化学反应中失去的电子越多,其还原性就越强 | |
| D. | 置换反应不一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 如图 1 所示,若铜中含有杂质银,可形成原电池,且铜作负极 | |
| B. | 如图 2 所示,当有 0.1 mol 电子转移时,有 0.1 mol Cu2O 生成 | |
| C. | 基于绿色化学理念设计的制取 Cu2O 的电解池如图 2 所示,铜电极发生还原反应 | |
| D. | 若图 3 所示的装置中发生 Cu+2Fe3+═Cu2++2Fe2+的反应,则 X 极是负极,Y 极的材料可 以是铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com