
| A. | 碳酸钠 | B. | 氢氧化钠 | C. | 氧化钠 | D. | 过氧化钠 |
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:实验题
 测定室温下NH3•H2O的浓度及电离平衡常数Kb
测定室温下NH3•H2O的浓度及电离平衡常数Kb查看答案和解析>>
科目:高中化学 来源: 题型:选择题
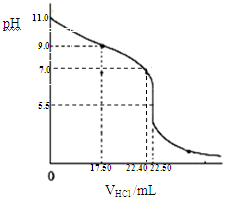
 25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )| A. | 在上述三种盐原溶液中,水的电离程度大小是NaX>NaY>NaZ | |
| B. | 在等物质的量浓度的NaX、NaY、NaZ混合液中,离子浓度的大小关系是c(Z-)>c(Y-)>c(X-) | |
| C. | 在上述NaX和NaY的混合液中存在$\frac{c(HX)}{c({X}^{-})}$=$\frac{c(HY)}{c({Y}^{-})}$ | |
| D. | 在0.2mol•L-1 NaX溶液中加 入等体积0.1mol•L-1的盐酸,所得混合液中存在c(H+)+c(HX)=c(OH-)+c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
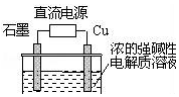 Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图,电解总反应:2Cu+H2O$\frac{\underline{\;通电\;}}{\;}$Cu2O+H2↑.下列说法正确的是( )
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图,电解总反应:2Cu+H2O$\frac{\underline{\;通电\;}}{\;}$Cu2O+H2↑.下列说法正确的是( )| A. | 石墨电极上产生氧气 | |
| B. | 铜电极发生还原反应 | |
| C. | 铜电极接直流电源的正极 | |
| D. | 当有0.1mol电子转移时,有0.1molCu2O生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40 g NaOH溶于水配成1 L溶液,其浓度为l mol•L-1 | |
| B. | 将22.4 L HC1溶于水配成1 L溶液,其浓度为lmol•L-1 | |
| C. | 1 L含2 mol K+的K2SO4溶液中K2SO4的浓度为1mol•L-1 | |
| D. | 将浓度为0.5 mol.L-l的NaNO3溶液100 mL恒温蒸发至50 mL,其浓度变为1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③④ | C. | ②④ | D. | ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com