

| A. | 干燥Cl2 | B. | 配制硫酸溶液 | C. | 蒸馏 | D. | 分液 |
分析 A.干燥气体导管应长进短出;
B.不能在容量瓶中稀释浓硫酸;
C.蒸馏时测定馏分的温度;
D.分液漏斗分离分层的液体.
解答 解:A.干燥气体导管应长进短出,图中干燥气体时进气方向不合理,不能干燥氯气,故A错误;
B.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释、冷却后转移到容量瓶中,故B错误;
C.蒸馏时测定馏分的温度,则温度计的水银球应在烧瓶的支管口处,故C错误;
D.分液漏斗分离分层的液体,则图中分液漏斗中液体分层,可分液,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握装置的作用、混合物分离提纯实验操作等为解答的关键,侧重分析与实验应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 23.3g | 19.7g |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸型酸雨的形成会涉及反应:2H2SO3+O2$\frac{\underline{\;催化剂\;}}{\;}$2H2SO4 | |
| B. | 氯化铝溶液中加入过量的氨水 Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| D. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3溶液加水稀释后,pH和KW均减小 | |
| B. | 0.1mol•L-1Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| C. | 浓度分别为0.2mol•L-1和0.1mol•L-1的CH3COOH溶液中,c(H+)之比等于2:1 | |
| D. | 室温下,PH=12的氨水与PH=2的H2SO4溶液等体积混合后,溶液呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
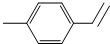 (写出分子式)C9H10
(写出分子式)C9H10查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com