
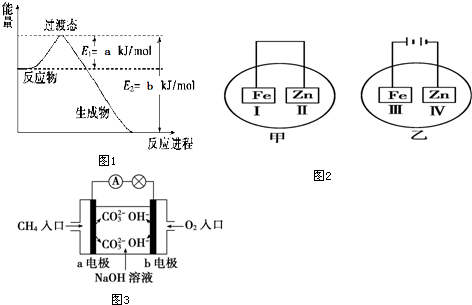
分析 (1)根据图象中能量变化,写出热化学方程式并标明物质聚集状态;
(2)据已知热化学方程式,利用盖斯定律解答;
(3)将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,甲形成原电池反应,锌为负极,铁为正极;
乙为电解反应,铁为阳极被氧化生成亚铁离子,阴极发生还原反应生成氢气;
(4)①燃料电池中,负极上投放燃料,发生失电子发生氧化反应,正极上投放氧气,发生得电子的还原反应;
②根据该燃料电池工作时的总反应中消耗了电解质溶液中的氢氧根离子来回答.
解答 解:(1)图象中生成1mol氨气的能量变化为:aKJ/mol-bKJ/mol=(a-b)KJ/mol,该反应放热,热化学方程式为:N2(g)+3H2 (g)═2NH3(g)△H=2(a-b)kJ/mol,
故答案为:N2(g)+3H2 (g)═2NH3(g)△H=2(a-b)kJ/mol;
(2)已知:①C(s,石墨)+O2(g)═C02(g)△H1=-393.5kJ•mol-1
②2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
③2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
据盖斯定律,(①×4+②-③)÷2得:2C(s,石墨)+H2(g)=C2H2(g)△H=[4×(-393.5KJ/mol)+(-571.6KJ/mol)-(-2599KJ/mol)]÷2=226.7kJ•mol-1
,故答案为:226.7kJ•mol-1;
(3)将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,甲形成原电池反应,锌为负极,铁为正极;
正极反应的电极方程式为2H2O+O2+4e-═4OH-,乙为电解反应,铁为阳极被氧化生成亚铁离子,阴极发生还原反应生成氢气,电极方程式为2H++2e-═H2↑,
故答案为:2H2O+O2+4e-═4OH-;2H++2e-═H2↑;
(4)①甲烷燃料电池中,通入甲烷的电极a为原电池的负极,负极上是甲烷发生失电子的氧化反应,在碱性环境中电极反应式为:CH4+10OH--8e-═CO32-+7H2O,
故答案为:a;CH4+10OH--8e-═CO32-+7H2O;
②根据电池的两极反应,在转移电子一样的情况下,消耗了溶液中的氢氧根离子,所以溶液的碱性减弱,pH减小,
故答案为:减小.
点评 本题考查了热化学方程式书写、盖斯定律的应用、原电池和电解池原理以及甲烷燃料电池的工作原理知识,注意知识的迁移和应用是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | X2YZ4 | B. | XYZ3 | C. | X3YZ4 | D. | X4Y2Z7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .(不用注明条件)
.(不用注明条件)
 .(不用注明条件)
.(不用注明条件) .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操 作 | 现 象 | 解释或结论 |
| A. | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B. | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化,形成致密的氧化膜 |
| C. | 向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 该溶液中存在NH4+ |
| D. | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO和CH3OH | B. | CO2和H20 | C. | H2和CO2 | D. | CH3OH和H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 0.25mol/L CaCl2溶液 | B. | 50ml 1mol/L KCl溶液 | ||
| C. | 50ml 0.5mol/L NaCl溶液 | D. | 200mL 0.25mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2+H2O═HCl+HClO | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2Na+2H2O═4NaOH+H2↑ | D. | 2H2O═2H2↑+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 以下为五种有机物的有关信息,根据表中信息回答问题.
以下为五种有机物的有关信息,根据表中信息回答问题.| A | B | D | E | F |
| ①由C、H、O 三种元素组成的液体; ②与水任意比例互溶. | 其产量用来衡量一个国家的石油化工水平. | 比例模型为: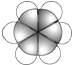 | ①可用于除水垢 ②在低于16.6℃时,凝固成冰一样的晶体. | 由5个原子组成的10个电子的共价分子. |
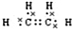 ,把一定体积的B、F混合气体通过溴水,有加成反应(填反应类型)发生,当溴水的质量增加2.8g时,生成物的质量为18.8g.(可能用到的相对原子质量:H 1;C 12;O 16;Br 80)
,把一定体积的B、F混合气体通过溴水,有加成反应(填反应类型)发生,当溴水的质量增加2.8g时,生成物的质量为18.8g.(可能用到的相对原子质量:H 1;C 12;O 16;Br 80)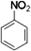 .
.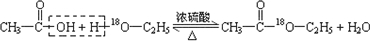 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 氧化还原反应 | C. | 置换反应 | D. | 分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com