
| A. | 50% | B. | 80% | C. | 88% | D. | 95% |
分析 在一定温度下,反应X(g)+Y(g)?2Z(g)的平衡常数为0.25,逆反应2Z(g)?X(g)+Y(g)平衡常数K=$\frac{1}{0.25}$=4,根据化学平衡三行计算,起始浓度为$\frac{10mol}{10L}$=1mol/L,设Z分解浓度为x,则
2Z(g)?X(g)+Y(g)
起始量(mol/L) 1 0 0
变化量(mol/L) x 0.5x 0.5x
平衡量(mol/L) 1-x 0.5x 0.5x
平衡常数K=$\frac{0.5x×0.5x}{(1-x)^{2}}$=4
x=0.8mol/L,该温度时达到平衡状态达到Z(g)的最大分解率.
解答 解:在一定温度下,反应X(g)+Y(g)?2Z(g)的平衡常数为0.25,逆反应2Z(g)?X(g)+Y(g)平衡常数K=$\frac{1}{0.25}$=4,根据化学平衡三行计算,起始浓度为$\frac{10mol}{10L}$=1mol/L,设Z分解浓度为x,则
2Z(g)?X(g)+Y(g)
起始量(mol/L) 1 0 0
变化量(mol/L) x 0.5x 0.5x
平衡量(mol/L) 1-x 0.5x 0.5x
平衡常数K=$\frac{0.5x×0.5x}{(1-x)^{2}}$=4
x=0.8mol/L,
该温度时达到平衡状态达到Z(g)的最大分解率=$\frac{0.8mol/L}{1mol/L}$×100%=80%,
故选B.
点评 本题考查了化学平衡、平衡常数计算,注意正逆反应的平衡常数互为倒数,注意知识的积累,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据是否有丁达尔效应,可将分散系分为溶液、胶体和浊液 | |
| B. | 含有最高价元素的化合物一定具有强氧化性 | |
| C. | NH3、SO2、SO3都是非电解质,氯化钠溶液、硫酸铜溶液都是电解质 | |
| D. | Na2CO3、NaHCO3、SiO2的俗称分别为纯碱、小苏打、硅石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 MOH和ROH两种一元碱,常温下其水溶液分别加水稀释时,pH变化如下图,下列说法正确的是( )
MOH和ROH两种一元碱,常温下其水溶液分别加水稀释时,pH变化如下图,下列说法正确的是( )| A. | 在x点,由HO电离出的c (H+)相等,c (M+)=c (R+) | |
| B. | 稀释前,c (ROH)=10 c (MOH) | |
| C. | 稀释前的ROH与等体积pH=1的H2SO4混合后所得溶液显酸性 | |
| D. | 等体积等浓度的MOH和HCl混合后,溶液中离子浓度大小关系:c (Cl-)>c (M+)>c (OH-)>c (H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸的化学式 | CH3COOH | HClO | H2CO3 |
| 电离常数 | 1.8×10-5 | 2.9×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 等物质的量浓度的各溶液①C(CH3COONa) ②C(NaClO) ③C(NaHCO3) ④C(Na2CO3)pH关系为:④>②>③>① | |
| B. | 少量CO2通入次氯酸钠溶液中:CO2+ClO-+H2O═HClO+HCO3- | |
| C. | 新制氯水中Cl2+H2O?HCl+HClO为适当增大HClO 的浓度,可加入少量固体Na2CO3 | |
| D. | 某浓度的NaClO溶液的pH=d,则其中由水电离出的c(H+)=10-dmol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸钠溶液和盐酸反应:HCOO-+H+═HCOOH | |
| B. | 硫化钠的第一步水解:S2-+2H2O?H2S+2OH- | |
| C. | 醋酸钡溶液和硫酸反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸氢钠的水解:HCO3-+H2O═H3O++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
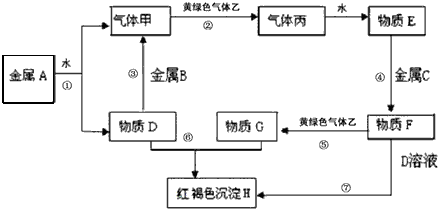
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 | |
| B. | 太阳能、煤气、潮汐能是一次能源:电力、蒸汽、地热是二次能源 | |
| C. | 吸热反应就是反应物的总能量比生成物的总能量小的反应:也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量少的反应 | |
| D. | CO(g)的燃烧热是283.0kJ/mol则2CO2(g)=2CO(g)+O2(g) 反应的△H=+566.0kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中加入少量固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+cOH-) | |
| B. | pH=9的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1mol•L-1CH3COOH溶液与0.05mol•L-1NaOH溶液等体积混合:2c(H+)+c((CH3COOH)=c(CH3COO-)+2c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com