


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
A、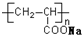 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| B、用于现代建筑的钢筋混凝土不属于复合材料 |
| C、pH=2的盐酸和NH4Cl溶液中,水电离出的c(H+)相等 |
| D、常温时铝遇浓硝酸钝化,是由于铝元素有很强的金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、78g苯分子中含有的碳碳双键数为3NA |
| B、7.8g Na2O2含有的阴离子数目为0.2NA |
| C、12g石墨烯(也就是单层石墨)中含有六元环的个数为NA |
| D、常温常压下,2g D216O中含中子数、质子数、电子数均为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和冷水反应 Na+2H2O═Na++2OH-+H2↑ |
| B、Fe片浸泡在FeCl3溶液中:Fe3++Fe═2Fe2+ |
| C、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+═BaSO4↓ |
| D、氯化铝溶液中加入过量的氨水 Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.05mol/L |
| B、0.1mol/L |
| C、0.2mol/L |
| D、0.3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com