
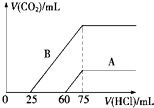
 ȡ�����ʵ���Ũ�ȵ�NaOH��Һ����A��B��ÿ��10mL���ֱ���A��B��ͨ�벻������CO2���ټ���������Һ����μ���0.1mol/L�����ᣬ��״���²�����CO2������������������֮��Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
ȡ�����ʵ���Ũ�ȵ�NaOH��Һ����A��B��ÿ��10mL���ֱ���A��B��ͨ�벻������CO2���ټ���������Һ����μ���0.1mol/L�����ᣬ��״���²�����CO2������������������֮��Ĺ�ϵ��ͼ��ʾ���Իش��������⣺| 0.0075mol |
| 0.01L |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij�¶�ʱ����2L������ijһ��Ӧ��A��B�������ʵ�����ʱ��仯��������ͼ��ʾ����ͼ�����ݷ����ã�
ij�¶�ʱ����2L������ijһ��Ӧ��A��B�������ʵ�����ʱ��仯��������ͼ��ʾ����ͼ�����ݷ����ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͭ�� | B��ͭ�ۺ�þ�ۻ�ϣ������£� |
| C��ˮ�� | D��Ӳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ���������� | ʵ��Ŀ�� |
| A | ��AlCl3��Һ�м��������NaOH��Һ�����ˣ�ϴ�ӣ������������ | ��ȡAl2O3 |
| B | �ñ��͵�Na2CO3��Һ���Խ�BaSO4ת��ΪBaCO3 | ֤��Ksp��BaSO4����Ksp��BaCO3�� |
| C | ���Ȼ��������м�������MgCl2��Һ | ��ȡ��ˮMgCl2 |
| D | ��SO2ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ��������ɫ���Ʒ����Һ����Һ�ָ���ɫ | ��֤H2SO3�IJ��ȶ��� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com