
����Ŀ�����仯�����ڹ�ҵ����������;�����������Ҫ�ɷ�ΪMg2B2O5��H2O��Fe3O4����������Fe2O3��FeO��CaO��Al2O3��SiO2��)Ϊԭ���Ʊ�����(H3BO3)�Ĺ���������ͼ��ʾ��

�ش��������⣺
��1��д��Mg2B2O5��H2O�����ᷴӦ�Ļ�ѧ����ʽ_____________��Ϊ��߽������ʣ����ʵ���������Ũ��Ũ���⣬���ɲ�ȡ�Ĵ�ʩ��_________��д����������
��2������ �Ĵ��ԣ��ɽ�������������з��롣���������л�ʣ���������______��д��ѧʽ����
��3�����������������ȼ�H2O2��Һ��������_______�� Ȼ���ٵ�����Һ��pHԼΪ5��Ŀ����________��
��4�������������е���Ҫ������ �������ƣ���
��5��������Ϊԭ�Ͽ��Ƶ����⻯�ƣ�NaBH4���������л��ϳ��е���Ҫ��ԭ���������ʽΪ_______��
��6����������������ɾ������������������֡�������ͽ���þΪԭ�Ͽ��Ʊ��������û�ѧ����ʽ��ʾ�Ʊ�����___________��
���𰸡���1�� Mg2B2O5��H2O+2H2SO4![]() 2MgSO4+2H3BO3����С��������������߷�Ӧ�¶ȡ�
2MgSO4+2H3BO3����С��������������߷�Ӧ�¶ȡ�
��2�� Fe3O4�� SiO2��CaSO4��
��3����Fe2+����ΪFe3+��ʹAl3+��Fe3+�γ������������ȥ��
��4������ˮ������þ
��5��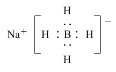
��6�� 2H3BO3 ![]() B2O3+3HO B2O3+3Mg
B2O3+3HO B2O3+3Mg ![]() 3MgO+2B
3MgO+2B
����������1����д��ѧ����ʽ���Ƿ��ռ�ʽ̼���κ���ķ�Ӧ������Ҫ�ȷ���Mg2B2O5��H2O ����Ԫ�صĻ��ϼ�Ϊ+3�ۣ���ϵ������ͼ���ղ������֪����Ԫ�ر�ΪH3BO3��H3BO3Ϊ���ᣬ������ˮ�����ⲻ��������ԭ��Ӧ����þԪ��ת��Ϊ����þ���ӿ췴Ӧ���ʿ��Բ������µȴ�ʩ�������������ĽӴ����Ҳ����ѧ���档
��2����ϵ���д���ֻ��Fe3O4������дFe3O4����ѧ��ѧ��Ӧ�������ſ�������ʣ�µIJ��������SiO2����CaSO4��
��3���Ƚ���Һ�е�Fe2+����ΪFe3+���ٵ�����Һ��pH���Գ�ȥ��Һ�е�Al3+��Fe3+�����Ǹ�������ѵ���ij��ӷ�����
��4�����н���������þ��ĸҺ��Ӧ�������뵽����þҲ��ᾧ������ֻ�Ǿ��庬���߸��ᾧˮ�������뵽������ˮ����п����ˮ�����������룩��������þ����Ӧ��Ҳ���ԡ�
��5�����⻯�Ƶĵ���ʽ�ܲ����棬����ʽ�������Ӽ����������ڲ��Ĺ��ۼ������ֺϳɡ�
��6������ʱ�����룬�����Ӧ���¶�Ӧ�ñȽϸߣ�����H3BO3��ֽ⣬Ȼ������û���Ӧ���ٽ���ѧ����ʽ��ƽ�ͺá�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ʶ����ʱ���õĿ�ѧ���������й���̼��ط����˵�������������
A�����ڵ����
B�����ڻ�����
C������̼����
D�����ڷ�ɢϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ſƼ��Ľ���������������Դ������������Ϊ��������ע�Ľ���
��1�����������ˮ�帻Ӫ��������Ҫ����֮һ���ô�������ˮ�����ɵĴ����Ὣˮ�еİ�������NH3��ʾ��ת��Ϊ������ȥ������ط�Ӧ����Ҫ�Ȼ�ѧ����ʽ���£�
��Ӧ�٣�NH3��aq��+HClO��aq��= NH2Cl��aq��+H2O��l����H1= akJmol��1
��Ӧ�ڣ�NH2Cl��aq��+HClO��aq��= NHCl2��aq��+H2O��I����H2= bkJmol��1
��Ӧ�ۣ�2NHCl2��aq��+H2O��l��= N2��g��+HClO��aq��+3HCl��aq����H3= ckJmol��1
�� 2NH3��aq��+3HClO��aq��= N2��g��+3H2O��I��+3HCl��aq���ġ�H=______��
�� ��ҺpH�Դ�������ȥ�������нϴ��Ӱ�죨��ͼ1��ʾ������pH�ϵ�ʱ��Һ������ɫ��ζ���������ɣ�����ȥ��Ч�ʽϵͣ���ԭ����_________________��
�� �õ绯ѧ��Ҳ����ȥ����ˮ�а�����������ˮ�м���������ö��Ե缫ֱ�ӵ�ⷢ�ְ���ȥ��Ч�ʼ��ͣ�������Һ���ټ���һ�������Ȼ��ƺ�ȥ��Ч�ʿ��Դ����ߡ���Ӧװ����ͼ2��ʾ��bΪ�缫__�������ʱ�����ĵ缫��ӦʽΪ_____________��

��2������̼���á�����Ϊ��ѧ���о�����Ҫ���⡣
�� �Զ������ѱ��渲��Cu2Al2O4 Ϊ���������Խ�CO2 ��CH4 ֱ��ת�������ᡣ�ڲ�ͬ�¶��´����Ĵ�Ч���������������������ͼ��ʾ��250��300 ��ʱ���¶����߶�������������ʽ��͵�ԭ����__________________��
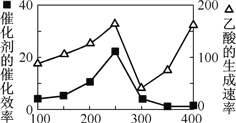
�� Ϊ����߸÷�Ӧ��CO2��ת���ʣ����Բ�ȡ�Ĵ�ʩ��_____________����дһ�����ɣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ����Ƽ����Ӧ�����ӷ���ʽ����ȷ���ǣ� ��
A. ����������ˮ�Ʊ������Cl2+H2O��2H++Cl��+ClO��
B. ˮ�����ڿ����б��ʣ�Na2SiO3+CO2+H2O��2Na++CO32-+H2SiO3��
C. ��FeCl3��Һ��ʴͭ��·�壺Cu+2Fe3+��Cu2++2Fe2+
D. ��Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO![]() +6H++5H2O2��2Mn2++5O2��+8H2O
+6H++5H2O2��2Mn2++5O2��+8H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2016�������һ�е��Ĵ��¿��������仯�������ճ����������Ӧ�ù㷺��
��1���������ƣ�Na2FeO4����ˮ���������е�һ�����;�ˮ������ҵ������NaClO ��NaOH�Ļ����Һ��2Fe��OH��3�������Ʊ��������ƣ���Ӧ�Ļ�ѧ����ʽΪ �������������������;�ˮ����ԭ���� ��
��2�������������ϸ�ijЩ���ϻ�ϣ������Ƴɷ������ᡣ�Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȣ����������Ʊ����죨Fe2O3���Ĺ������£�
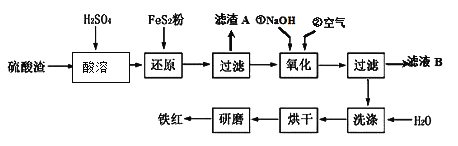
�����ܹ����з�����Ӧ�Ļ�ѧ����ʽΪ �� �� ��������A����Ҫ�ɷݵĻ�ѧʽΪ ��
����ԭ�����м���FeS2��Ŀ���ǽ���Һ�е�Fe3 +��ԭΪFe2 +��������������ΪH2SO4����д���÷�Ӧ�����ӷ���ʽ ��
�����������У�O2��NaOH��Fe2+��Ӧ�����ӷ���ʽΪ ��
��Ϊ��ȷ������������ʹ��ȣ�����������Ҫ������Һ��pH�ķ�Χ�� ��
������ | Fe��OH��3 | Al��OH��3 | Fe��OH��2 | Mg��OH��2 |
��ʼ����pH | 2.7 | 3.8 | 7.6 | 9.4 |
��ȫ����pH | 3.2 | 5.2 | 9.7 | 12.4 |
���pH������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������в����ڣ� ��
A. ���Ӽ� B. ���Լ� C. �Ǽ��Լ� D. ���Ӽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2015�������ۻ�ѧ����ͨ����н�������ʵ�飺
���� |
|
| |
���� | Fe�������������ɫ���ݣ�Һ���Ϸ���Ϊ����ɫ | Fe���������������ɫ���ݺ�Ѹ��ֹͣ | Fe��Cu�Ӵ���������������ɫ���� |
����˵��������ȷ���� �� ��
A��������������ɫ�����ɫ�Ļ�ѧ����ʽΪ��2NO+O2=2NO2
B�����е�����˵��Fe�����γ����ܵ������㣬��ֹFe��һ����Ӧ
C���Ա�������������˵��ϡHNO3��������ǿ��ŨHNO3
D���������������Fe��Cu֮�����ӵ����ƣ����ж�Fe�Ƿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2017����ģ�������й��ڷ�Ӧ���ʵ�˵��������ǣ� ��
A����Ӧ�������ں�����ѧ��Ӧ���еĿ���
B�����淴Ӧ�ﵽ��ѧƽ��״̬ʱ�������淴Ӧ���ʶ�Ϊ0
C��������Ӧ���ʵ���Ҫ�����Ƿ�Ӧ�������
D������Ӧ��Ũ�ȣ���߷�Ӧ�¶ȶ�������Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ħ�������������������ȷ���� (����)
A. ����Ħ������ǵ�λ���ʵ�����������ռ�����
B. ��״���£�����Ħ�����ԼΪ22.4 L
C. ��״���£�1 mol�κ�������ռ�����Լ��22.4 L
D. ��״���£�1 mol������ռ�����Լ��22.4 L��mol��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com