
����Ŀ��ʵ�����ù����ռ�����0.4mol/L��NaOH��Һ480mL��0.5mol/L��������Һ500mL����ش�
��1��������ҪNaOH��������g��
��2�����������������ձ� ��ҩ�� ��250mL����ƿ ��500mL����ƿ �ݲ�������������ƽ ����Ͳ����������������Һ����ʹ�õIJ�������������ţ�����ȱ�ٵ������� ��
��3�����ݼ����֪��������Ͳ��ȡ��������Ϊ98%���ܶ�Ϊ1.84g/cm3��Ũ��������ΪmL�����ʵ������15mL��20mL��50mL��Ͳ��Ӧѡ��mL��Ͳ��ã�
��4�����ƹ����У����в�����������ƫ�ߵ���������ţ�
��δϴ���ձ��������� �ڳ���NaOH��ʱ��̫��
�۶���ʱ���ӿ̶� ������ƿ�����������������ˮ
��NaOH��Һδ��ȴ�����¾�ת�Ƶ�����ƿ ����ȡŨ����ʱ��������Ͳ�̶��ߣ�
���𰸡�
��1��8.0
��2���٢ڢܢݢޢ�,��ͷ�ι�
��3��13.6,15
��4���ۢݢ�
���������⣺��1�������ռ�����0.4mol/L��NaOH��Һ480mL��Ӧѡ��500mL����ƿ��ʵ������500mL��Һ����Ҫ��������������0.4mol/L��0.5L��40g/mol=8.0g��
�ʴ�Ϊ��8.0��
��2��û�й��Ϊ480mL������ƿ������ʱ��Ҫѡ��500mL������ƿ�����Ʋ���Ϊ�����㡢��������ȡ�����ܽ⣨ϡ�ͣ�����ȴ��ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ���Ҫʹ�õ������У�������ƽ����Ͳ�������������ձ���ҩ�ס�500mL����ƿ����ͷ�ιܵȣ����Ա����õ����������٢ڢܢݢޢߣ���ȱ�ٵ���������ȱ�ٵIJ�������Ϊ����ͷ�ιܣ�
�ʴ�Ϊ���٢ڢܢݢޢߣ���ͷ�ιܣ�
��3��98%���ܶ�Ϊ1.84g/cm3��Ũ�������ʵ���Ũ��C= ![]() =18.4mol/L������ҪŨ�������ΪV����������Һϡ���������ʵ����ʵ�������ã�18.4mol/L��V=0.5mol/L��500mL�����V=13.6mL����ȡ13.6mL��Һ��Ӧѡ��15mL��Ͳ��
=18.4mol/L������ҪŨ�������ΪV����������Һϡ���������ʵ����ʵ�������ã�18.4mol/L��V=0.5mol/L��500mL�����V=13.6mL����ȡ13.6mL��Һ��Ӧѡ��15mL��Ͳ��
�ʴ�Ϊ��13.6��15��
��4����δϴ���ձ������������������ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ��ʲ�ѡ��
�ڳ���NaOH��ʱ��̫�������³�ȡ�Ĺ�����������������ƫС�����ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ��ʲ�ѡ��
�۶���ʱ���ӿ̶ȣ�������Һ���ƫС����ҺŨ��ƫ�ߣ���ѡ��
������ƿ�����������������ˮ�������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ�Ȳ��䣬�ʲ�ѡ��
��NaOH��Һδ��ȴ�����¾�ת�Ƶ�����ƿ����ȴ����Һ���ƫС����ҺŨ��ƫ�ߣ���ѡ��
����ȡŨ����ʱ��������Ͳ�̶��ߣ�������ȡŨ�������ƫ�����ʵ����ʵ���ƫ����ҺŨ��ƫ�ߣ���ѡ��
��ѡ���ۢݢޣ�
��1��ʵ������û��480mL����ƿ��������Ҫ����500mLNaOH��Һ���ݴ˼�����ҪNaOH��������
��2���������ù�����������һ�����ʵ���Ũ�ȵ���Һ�IJ����ж���Ҫ��������
��3��������Һϡ�Ͷ��ɼ�����ҪŨ����������
��4������![]() ������Һ����������ʵ����ʵ����仯����.
������Һ����������ʵ����ʵ����仯����.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ��֤���彡��������ʱ��Ҫ��ҩ����ҩƷͨ�������������ã����и����á��ݴ˻ش�
��1����ҵ���Ʊ���˾ƥ�ֵķ�Ӧ����ʽΪ��
��2����Ƽ���һ������֧�����������в�ҩ�������и����ã���������
��3������ҩ������θ������һ��ҩƷ����д���������ֿ���ҩ�к�θ�ᷴӦ�����ӷ���ʽ��
��Al(OH)3����
��NaHCO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Խ����У���MnSO4��Һ��μӣ�NH4��2S2O8����������泥���Һ�ᷢ�����·�Ӧ��Mn2++S2O82��+H2O��MnO4��+SO42��+H+ �� ����˵������ȷ���ǣ� ��
A.�������ø÷�Ӧ����Mn2+
B.�����ԱȽϣ�S2O82����MnO4��
C.�÷�Ӧ�����Խ��ʿ���Ϊ����
D.����0.1mol�����������ɣ���ת�Ƶ���0.5mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ag2CrO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ��t��ʱ����ӦAg2CrO4��s��+2Cl����aq��=2AgCl��s��+CrO42����aq����K=2.5��107 �� ����˵����ȷ���ǣ�������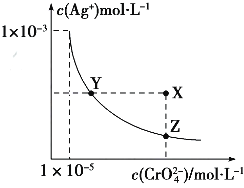
A.t��ʱ��Ag2CrO4��KspΪ1��10��12
B.t��ʱ����Ag2CrO4��Һ�м���K2CrO4��Һ���ٴ�ƽ��ʱc2��Ag+����c��CrO42������Ksp
C.t��ʱ��Ksp��AgCl��=1.56��10��10
D.t��ʱ����0.01molL��1 AgNO3��Һ�ζ�20mL 0.01molL��1KCl��0.01mol K2CrO4�Ļ����Һ��CrO42���ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ǰ�߸պ��Ǻ����������ǣ�������
A.2 molˮ��Ħ��������1 molˮ��Ħ������
B.200 mL 1 mol/L�Ȼ�����Һ��c��Cl������100 mL 2 mol/L�Ȼ�����Һ��c��Cl����
C.64 g������������ԭ�����ͱ�״����22.4 Lһ����̼����ԭ����
D.20%NaOH��Һ��NaOH�����ʵ���Ũ�Ⱥ�10%NaOH��Һ��NaOH�����ʵ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����18.6g Fe��Zn�Ͻ��м���200mLijŨ�ȵ�ϡ����ǡ����ȫ��Ӧ������0.3mol H2 �� ��ԭ�Ͻ�����mol Fe��ϡ��������ʵ���Ũ��Ϊ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ǣ������� ��NaHCO3��Һ��ˮϡ�ͣ�c��Na+��/c��HCO3������ֵ��������
��Ũ�Ⱦ�Ϊ0.1molL��1��Na2CO3��NaHCO3�����Һ��2c��Na+��=3[c��CO32����+c��HCO3����]
����0.1molL��1��ˮ�еμ�0��lmolL��1���ᣬǡ����ȫ��Ӧʱ��Һ��pH=a������ˮ���������c��OH����=l0��amolL��1
����0.1molL��1��NH4��2SO3��Һ�м�������NaOH���壬c��Na+����c��NH4+����c��SO32����������
����Na2Sϡ��Һ�У�c��OH����=c��H+��+2c��H2S��+c��HS����
A.�٢�
B.�ڢ�
C.�٢�
D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ͬѧ�����÷���м��������ͭ���ʣ���̽���Ʊ�FeCl36H2O�ķ�����ͬѧ����Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ��������ϡ���ᣬʵ��ʱ�ȴ�a���ر�b���÷�Һ©����A�м�������������ַ�Ӧ����ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl36H2O���壮 ��д���пհף�
��1���μ�����ʱ�����ַ�Ӧ���ʽ�֮�����봿���۷�ӦҪ�죬��ԭ���� ��
��2���ձ��ڷŹ���ϡHNO3��ԭ�����������ӷ���ʽ��ʾ����
��3������ʵ������У����ɼ�a���������Ϊ�ų������������⣬��һ��Ŀ���� ��
��4����ͬѧ�Ը�ʵ������˸Ľ��������ÿ��ձ�ʢ����Һ�������ʵ����Լ���Ȼ����HC1�������С�һ���¶���������Ũ�������½ᾧ���õ�������FeCl36H2O������Ϊ������Լ������� �� ������ţ� ���������� ���������������ϡ����
�����Ը��������Һ ������������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ʵ������У���ȷ���ǣ� ��
A.�������ƿ�Ƿ�©ˮ
B.����Һ����
C.�μ�Һ��![]()
D.����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com