
 二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是( )
二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是( )| A、二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 |
B、1mol环戊二烯(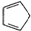 )中含有σ键的数目为5NA )中含有σ键的数目为5NA |
| C、分子中存在π键 |
| D、Fe2+的电子排布式为1s22s22p63s23p63d44s2 |
 )分子中含有σ键的数目为13;
)分子中含有σ键的数目为13; )分子中含有σ键的数目为13,则1mol环戊二烯(
)分子中含有σ键的数目为13,则1mol环戊二烯( )中含有σ键的数目为13NA,故B错误;
)中含有σ键的数目为13NA,故B错误;

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
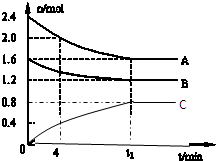 T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.| n(A) |
| n(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2-溴丁烷 |
| B、3,3-二甲基-2-氯戊烷 |
| C、2,2-二甲基-1-氯丁烷 |
| D、1,3-二氯苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
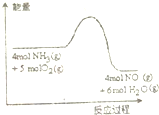 一定条件下密闭容器中发生如图反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)反应过程中能量变化如图所示,下列说法正确的是( )
一定条件下密闭容器中发生如图反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)反应过程中能量变化如图所示,下列说法正确的是( )| A、降低温度可以加快正反应速率 |
| B、反应体系中加入催化剂可增加反应热 |
| C、降低温度可以提高NH3的转化率 |
| D、增加空气的量可以提高混合气体中NO的体积分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O+H2O?H3O++OH- |
| B、HCO3-+H2O?H2CO3+OH- |
| C、HCO3-+H2O?H3O++CO32- |
| D、HCO3-+OH-?H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-… | Cl2、Mn2+… |
| A、反应①的其余产物为H2O和O2 |
| B、反应②中Cl2与FeBr2的物质的量之比为1:2 |
| C、反应③中生成1 mol Cl2,转移电子2 mol |
| D、氧化性由强到弱的顺序为Cl2>MnO4->Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
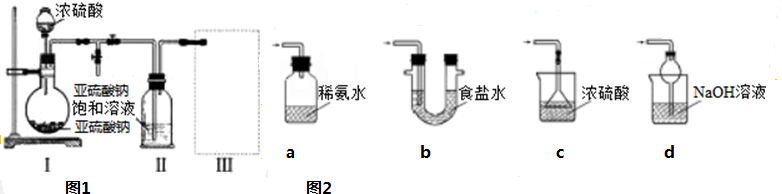

查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH/H2O |
| NaOH/醇 |
| 加热 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com