
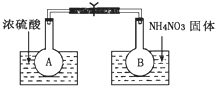
 ��֪2NO2��g���TN2O4��g����H��298K��=-52.7kJ•mol-1��ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬������������ʵ�飺
��֪2NO2��g���TN2O4��g����H��298K��=-52.7kJ•mol-1��ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬������������ʵ�飺���� ��1��Ũ����ϡ��ʱ�ų�������������Һ���¶����ߣ�������ܽ�ʱ����������������Һ���¶Ƚ��ͣ������¶�ƽ�������ȷ����ƶ��������¶ȣ�ƽ������ȷ����ƶ���
��2������������ɫ�ı仯ȷ���ƶ�����
��3��Kc=$\frac{c��{N}_{2}{O}_{4}��}{{c}^{2}��N{O}_{2}��}$�������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�������ƽ���ƶ�����ȷ������������ת���ʣ�
��� �⣺��1��Ũ����ϡ��ʱ�ų�������������Һ���¶����ߣ�������ܽ�ʱ����������������Һ���¶Ƚ��ͣ���Ӧ2NO2��g��?N2O4��g���Ƿ��ȷ�Ӧ��A�ձ��У������¶ȣ�ƽ�����淴Ӧ�����ƶ���������������Ũ������������ɫ��������¶ȣ�ƽ��������Ӧ�����ƶ�����������Ũ�Ƚ��ͣ�����������ɫ��dz���ʴ�Ϊ��������ɫ���������ɫ��dz��
��2�������Ϸ���֪�������¶ȣ�ƽ��������Ӧ�����ƶ����ʴ�Ϊ������
��3��Kc=$\frac{c��{N}_{2}{O}_{4}��}{{c}^{2}��N{O}_{2}��}$�������¶ȣ�ƽ�����淴Ӧ�����ƶ������¶�������ת���ʽ��ͣ�
�ʴ�Ϊ��Kc=$\frac{c��{N}_{2}{O}_{4}��}{{c}^{2}��N{O}_{2}��}$����С��
���� ���⿼�����¶ȡ�ѹǿ�Ի�ѧƽ���Ӱ�죬�ѶȲ�������������ԭ����������ɣ�


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ȡ����Ӧ��
������ȡ����Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| װ�� | B | F | G |
| ʵ������ | |||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ����I | ������ | �ж� |
| A | ͭ�̵���Ҫ�ɷ��Ǽ�ʽ̼��ͭ | ����ϡ�����ͭ�������ͭ�� | ��ԣ���� �� |
| B | ͭ�̵���Ҫ�ɷ��Ǽ�ʽ̼��ͭ | ͭ����������ʢ��Ũ���� | I�ԣ���ԣ��� |
| C | ������ͭ��Һͨ����������������ɫ�������������˺���������������ɺ�ɫ���� | ��ͭ˿���ھƗ��ƻ���������ͭ˿������ | I�ԣ���ԣ��� |
| D | ��ɫ����ͭ��������ת��Ϊ��ɫ����ͭ��ĩ�������仯 | ����ͭ��Һ��������Ӿ�ص������� | ������ԣ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 28 g�������е�ԭ����ΪNA | |
| B�� | 4 g�����Ʊ�ɸ�����ʱʧȥ�ĵ�����Ϊ0.1NA | |
| C�� | 1 mol O2���ӵ���������1 mol��ԭ�ӵ����� | |
| D�� | 24 g O2���Ӻ�24 g O3������������ԭ����Ŀ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com