
使用SNCR脱硝技术的原理是![]() ,下图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
,下图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是
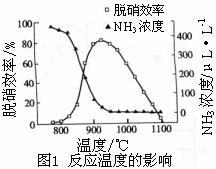
A.从图1判断,该反应的正反应方向是放热反应
B.从图1判断,脱硝的最佳温度约为925℃
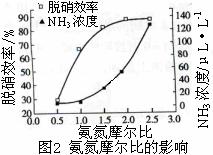
C.从图2判断,减少氨气的浓度有助于提高NO的转化率
D.从图2判断,综合考虑脱硝效率和运行成本最佳氨氮摩尔比应为2.5
科目:高中化学 来源: 题型:
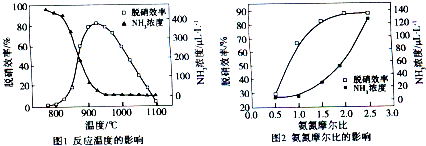
| A、从图1判断,该反应的正反应方向是放热反应 | B、从图2判断,减少氨气的浓度有助于提高NO的转化率 | C、从图1判断,脱硝的最佳温度约为925℃ | D、从图2判断,综合考虑脱硝效率和运行成本最佳氨氮摩尔比应为2.5 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省长沙市高三第四次月考化学试卷(解析版) 题型:填空题
SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:
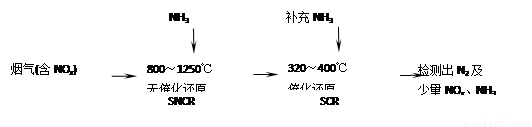
(1)反应2NO+2CO 2CO2+N2能够自发进行,则该反应的ΔH 0(填“>”或“<”)。
2CO2+N2能够自发进行,则该反应的ΔH 0(填“>”或“<”)。
(2)SNCR-SCR流程中发生的主要反应有:
①4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g) ΔH=-1627.2kJ•mol-1;
4N2(g)+6H2O(g) ΔH=-1627.2kJ•mol-1;
②6NO(g)+4NH3(g) 5N2(g)+6H2O(g) ΔH=-1807.0 kJ•mol-1;
5N2(g)+6H2O(g) ΔH=-1807.0 kJ•mol-1;
③6NO2(g)+8NH3(g) 7N2(g)+12H2O(g) ΔH=-2659.9 kJ•mol-1;
7N2(g)+12H2O(g) ΔH=-2659.9 kJ•mol-1;
反应N2(g)+O2(g) 2NO(g)的ΔH=
kJ•mol-1。
2NO(g)的ΔH=
kJ•mol-1。
(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图。
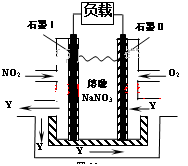
该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为:
(4)可利用该电池处理工业废水中含有的Cr2O72-,处理过程中用Fe作两极电解含Cr2O72-的酸性废水,随着电解的进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀来除去Cr2O72-。
①写出电解过程中Cr2O72-被还原为Cr3+的离子方程式: 。
②该电池工作时每处理100L Cr2O72-浓度为0.002mol/L废水,消耗标准状况下氧气 L。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省苏锡常镇徐连六市高三3月教学情况调研(一)化学试卷(解析版) 题型:填空题
SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:
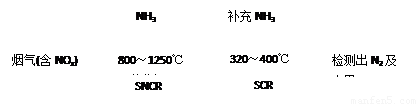
(1)反应2NO+2CO 2CO2+N2能够自发进行,则该反应的ΔH 0(填“>”或“<”)。
2CO2+N2能够自发进行,则该反应的ΔH 0(填“>”或“<”)。
(2)SNCR-SCR流程中发生的主要反应有:
4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g) ΔH=-1627.2kJ•mol-1;
4N2(g)+6H2O(g) ΔH=-1627.2kJ•mol-1;
6NO(g)+4NH3(g) 5N2(g)+6H2O(g) ΔH=-1807.0 kJ•mol-1;
5N2(g)+6H2O(g) ΔH=-1807.0 kJ•mol-1;
6NO2(g)+8NH3(g) 7N2(g)+12H2O(g) ΔH=-2659.9 kJ•mol-1;
7N2(g)+12H2O(g) ΔH=-2659.9 kJ•mol-1;
反应N2(g)+O2(g) 2NO(g)的ΔH=
kJ•mol-1。
2NO(g)的ΔH=
kJ•mol-1。
(3)NO和NH3在Ag2O催化剂表面的反应活性随温度的变化曲线见图。
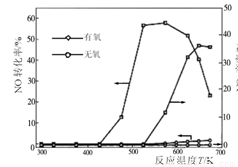
①由图可以看出,脱硝工艺流程应在 (填“有氧”或“无氧”)条件下进行。
②随着反应温度的进一步升高,在有氧的条件下NO的转化率明显下降的可能原因是 。
(4)NO2也可用尿素[CO(NH2)2]还原,写出尿素与NO2反应的化学方程式: 。
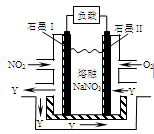
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图11。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。若生成1molY,则理论上需要消耗标准状况下氧气的体积为 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com