
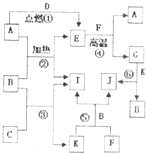
 ��ͼ����ѧ��ѧ��������֮���ת����ϵ������A��C��D��F��IΪ���ʣ�����Ϊ�����C��D�ڵ�ȼ�����ȵ����������ɵ���ɫ�Ĺ��壬B������ΪҺ̬���Իش������й����⣺
��ͼ����ѧ��ѧ��������֮���ת����ϵ������A��C��D��F��IΪ���ʣ�����Ϊ�����C��D�ڵ�ȼ�����ȵ����������ɵ���ɫ�Ĺ��壬B������ΪҺ̬���Իش������й����⣺
| ||
| 8 |
| 3 |
| ||
| 8 |
| 3 |


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д� ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ۢ� | B���ڢ� | C���٢� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ʵ����� | ʵ������ | ���� |
| A | ��ʢ��Fe��NO3��2��Һ���Թ��м���0.1mol/L H2SO4��Һ | �Թܿڳ��ֺ���ɫ���� | ��Һ��NO3-��Fe2+��ԭΪNO2 |
| B | ��Na2CO3��Һ��ͨ������CO2 | ��Һ����� | ����Na2CO3���� |
| C | �����pH=2��HX��HY������ֱ�������������Ӧ����ˮ���ռ����� | HX�ų����������ҷ�Ӧ���ʿ� | HX���Ա�HY�� |
| D | ����2mL0.1mol/LNa2S��Һ�еμ���0.1mol/LZnSO4��Һ���ټ��뼸��0.1mol/LCuSO4��Һ | ��ʼ�а�ɫ�������ɣ������к�ɫ�������� | Ksp��ZnS����Ksp��CuS�� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
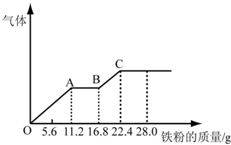 ijϡ�����ϡ����Ļ����Һ200mL��ƽ���ֳ����ݣ�������һ��������ͭ�ۣ�������ܽ�19.2g����֪����ֻ����ԭΪNO���壩������һ�����������ۣ�������������������������ӵı仯��ͼ��ʾ��
ijϡ�����ϡ����Ļ����Һ200mL��ƽ���ֳ����ݣ�������һ��������ͭ�ۣ�������ܽ�19.2g����֪����ֻ����ԭΪNO���壩������һ�����������ۣ�������������������������ӵı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
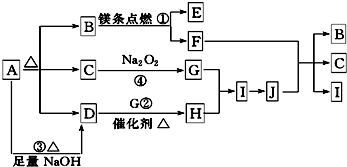
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������������ȼ�գ����ɰ�ɫ���� |
| B��ͭ˿��������ȼ�գ���������ɫ���Ȼ�ͭ |
| C����ȼ��ʹ�������������ϵ�Ψһ���� |
| D����������۽�����Ӧ���ɸ۽����Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��amol?L-Ԫ��HA��Һ��bmol?L-1NaOH��Һ�������Ϻ���pHΪ7����c��A-��=c��Na+�� |
| B����Kw/c��H+��=0.1mol?L-l����Һ�У�Na+��K+��CO32-��NO3-�ܴ������� |
| C������Ũ�ȵ������Na2CO3��Һ��CH3COONa��Һ��NaOH��Һϡ����ͬ������pH�仯������CH3COONa��Һ |
| D��25��ʱ�������Ƶζ���Ԫ����H2Rˮ��Һ���õ�����H2R��HR-��R2-����������Һ����c��Na+��=c��R2-��+c��HR-��+c��H2R��ʱ��Һ������ΪNaHR |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���٢ۢ� |
| C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CaO��C2H5OH |
| B��HCl��CH3COOH |
| C��H2S��BaSO4 |
| D��NH3?H2O��Cu |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com