
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
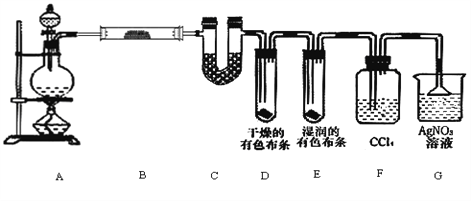
(1)若含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2 ,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是_______________________________________________。
(2)①装置B中盛放的试剂名称为__________,作用是________________________。装置C中盛放的试剂名称为_________________。
②装置D和E中出现的不同现象说明的问题是_________________________________。
③装置F的作用是_________________________。
④写出装置G中发生反应的离子方程式_____________________________________。
(3)为充分证明有氯化氢挥发出来,还应在装置F和G之间连接一个装有_________的广口瓶。
【答案】 浓盐酸的浓度随着反应的进行会变小,MnO2与稀盐酸不反应;加热时浓盐酸因挥发而损失 无水硫酸铜 证明有水蒸气产生 无水氯化钙 氯气无漂白性,次氯酸有漂白性 吸收氯气 Ag++Cl-===AgCl↓ 湿润的淀粉KI试纸(或湿润的有色布条)
【解析】(1)浓盐酸与足量MnO2反应制取Cl2,反应需要加热,氯化氢易挥发,反应消化氯化氢,同时生成水,随反应的不断进行浓盐酸的浓度逐渐变稀,稀盐酸不反应不与MnO2反应,所以制得的Cl2在标准状况下体积总是小于1.12L;(2)①硫酸铜吸水生成蓝色硫酸铜晶体,检验含有水蒸气,所以装置B中盛放的试剂名称为无水硫酸铜,作用是证明有水蒸气产生;要证明干燥的氯气不能漂白有色布条,则必须利用干燥剂干燥氯气,所以装置C中的试剂是无水氯化钙;②干燥的有色布条不褪色,说明氯气不具有漂白性;湿润的有色布条褪色,氯气与水反应生成盐酸与次氯酸,盐酸不具有漂白性,所以使有色布条褪色的物质是次氯酸,故次氯酸有漂白性;即装置D和E中出现的不同现象说明的问题是氯气无漂白性,次氯酸有漂白性;③氯气易溶于有机溶剂,四氯化碳吸收氯气,防止干扰G中氯化氢的检验;④氯化氢与硝酸银反应生成氯化银和硝酸,反应离子方程式为Ag++Cl-===AgCl↓;(3)氯气与水反应会生成盐酸,干扰G中氯化氢的检验,故在F、G之间加一装置,用湿润的淀粉KI试纸检验氯气是否被完全吸收。


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(A,B,C,D均为10电子微粒,组成它们的元素原子序数均小于10),下列说法正确的是( ) 
A.分子C与D不能发生化学反应
B.微粒A的空间结构与CH4相似,它们均为正四面体,所以A是非极性分子
C.固态D的熔沸点明显高于固态H2S的原因在于D分子中的共价键强于S﹣H键
D.在25℃时,A的盐酸盐溶液的pH小于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将阿伏加德罗常数规定为0.024kg12C中所含有的C原子数,而其他概念和规定一律不变,则下列各项的数值不会发生变化的是( )
A.物质的量
B.相对原子质量
C.物质的摩尔质量
D.12g12C中所含有的C原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向15 g铁和氧化铁的混合物中,加入200mL稀盐酸,在标准状况下放出氢气1.68 L,同时铁和氧化铁均无剩余;向溶液中滴加硫氰化钾溶液后,未见颜色变化。为了中和过量的盐酸,而且使Fe2+恰好完全转化成Fe(OH)2,共消耗2mol/L的NaOH溶液300 mL.
(1)生成氢气的质量为________g.
(2)加入300 mL NaOH溶液,反应后,溶液中的溶质主要是___________(填写化学式)。如不考虑混合后溶液体积变化,该溶质的物质的量浓度为__________.
(3)原盐酸中溶质的物质的量浓度是________________.
(4)原混合物中有铁__________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)m+np(填“>”“=”“<”).
(2)若加压时,A的质量分数 . (填“增大”“减小”或“不变”,下同)
(3)若加入A(体积不变),则B的转化率 .
(4)若降低温度,则平衡时B、C的浓度之比 ![]() 将 .
将 .
(5)若加入催化剂,平衡时气体混合物的总物质的量 .
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色(填“变深”“变浅”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一种固体化合物X,X本身不导电,但熔融状态或溶于水中能够电离,下列关于该化合物X的说法中,正确的是( )
A.X一定为电解质B.X固体不导电的原因一定是该固体中不存在离子
C.X只能是盐类D.X可以是任何化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为MnO2+ HCl(浓)![]() MnCl2 + Cl2↑+ H2O(未配平)。
MnCl2 + Cl2↑+ H2O(未配平)。
(1)配平上述反应:□MnO2+□ HCl(浓)![]() □MnCl2 + □Cl2↑+ □H2O________。
□MnCl2 + □Cl2↑+ □H2O________。
(2)在该反应中,如有1 mol Cl2生成,被氧化的HCl的物质的量是_____mol,转移电子的数目是_____mol。
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1∶1的混合液,反应的化学方程式是___________________________________。
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲观察环戊烯( ![]() )是否能使酸性KMnO4溶液褪色,先将环戊烯溶于适当的溶剂,再慢慢滴入0.005molL﹣1KMnO4溶液并不断振荡.下列哪一种试剂最适合用来溶解环戊烯做此实验( )
)是否能使酸性KMnO4溶液褪色,先将环戊烯溶于适当的溶剂,再慢慢滴入0.005molL﹣1KMnO4溶液并不断振荡.下列哪一种试剂最适合用来溶解环戊烯做此实验( )
A.四氯化碳
B.裂化汽油
C.甲苯
D.水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com