
����Ŀ��SO2��NOx����Ҫ�Ĵ�����Ⱦ�ijС����Ϊһ�������£���NH3��NO2��Ӧת��Ϊ����Ⱦ���ʿɽ�������β������������
��1���������Ʊ�
��ʵ�����ư����Ļ�ѧ����ʽΪ_________��
���Ʊ����ռ�����������İ���������ѡ����ͼװ��______(�����)��C���Լ�Ϊ______��

��2����������������ķ�Ӧ(��֪:2NO2+2NaOH=NaNO3+NaNO2+H2O��)
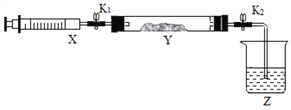
����Ӳ�ʲ�����Y�м���������������NO2����ע��Y���У�Z��Ӧʢװ______��
����K1����ע����X�е�NH3����ע��Y�У�������Ӧ�ķ���ʽΪ_______��
����ע���������˻�ԭ�����̶�����װ�ûָ������£���K2��Y�г��ֵ�������ԭ����_________��
��3����С���һ���о�SO2�����ʣ�̽��SO2�ܷ���Na2O2����������ԭ��Ӧ��ʵ������ͭ˿��Ũ���ᷴӦ����SO2�Ļ�ѧ����ʽΪ____________��������2����װ�ã���Y�е�ҩƷ����Ϊ����Na2O2����ע����X��SO2��������Y�У�Yװ���е���ɫ��ĩ��ɰ�ɫ����Ʒ����������ɵİ�ɫ�����к���SO42-_________��
���𰸡� 2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3�� ACDF��ACDCF ��ʯ�� NaOH��Һ 6NO2+8NH3
CaCl2+2H2O+2NH3�� ACDF��ACDCF ��ʯ�� NaOH��Һ 6NO2+8NH3![]() 7N2+12H2O ��Ӧ�����������������Y����ѹǿС����ѹ Cu+2H2SO4(Ũ)
7N2+12H2O ��Ӧ�����������������Y����ѹǿС����ѹ Cu+2H2SO4(Ũ)![]() CuSO4+2H2O+SO2�� ȡ������ɫ��������ˮ����������ϡ�������ټ���BaCl2��Һ����ɫ��������
CuSO4+2H2O+SO2�� ȡ������ɫ��������ˮ����������ϡ�������ټ���BaCl2��Һ����ɫ��������
����������1����ʵ�����ư����Ļ�ѧ����ʽΪ2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3�������Ʊ�������Ҫ���ȣ�ѡ��װ��A�����ﰱ����Ҫ��ʯ�ң���Ҫװ��C�������ܶ�С�ڿ�������������ˮ�������ռ�������Ҫװ��D��β��������Ҫ��������ѡ��װ��F����2����NO2�����Ǵ�����Ⱦ���Ҫβ����������Z��ӦʢװNaOH��Һ���ڰ����������������������ԭ��Ӧ���ɵ�����ˮ����Ӧ�ķ���ʽΪ6NO2+8NH3
CaCl2+2H2O+2NH3�������Ʊ�������Ҫ���ȣ�ѡ��װ��A�����ﰱ����Ҫ��ʯ�ң���Ҫװ��C�������ܶ�С�ڿ�������������ˮ�������ռ�������Ҫװ��D��β��������Ҫ��������ѡ��װ��F����2����NO2�����Ǵ�����Ⱦ���Ҫβ����������Z��ӦʢװNaOH��Һ���ڰ����������������������ԭ��Ӧ���ɵ�����ˮ����Ӧ�ķ���ʽΪ6NO2+8NH3![]() 7N2+12H2O�������ڷ�Ӧ��������������٣�Y����ѹǿС����ѹ�����Y�г��ֵ�����������3��ʵ������ͭ˿��Ũ���ᷴӦ����SO2�Ļ�ѧ����ʽΪCu+2H2SO4(Ũ)
7N2+12H2O�������ڷ�Ӧ��������������٣�Y����ѹǿС����ѹ�����Y�г��ֵ�����������3��ʵ������ͭ˿��Ũ���ᷴӦ����SO2�Ļ�ѧ����ʽΪCu+2H2SO4(Ũ)![]() CuSO4+2H2O+SO2��������SO42-һ���������ữ���Ȼ�����Һ����ʵ�鷽����ȡ������ɫ��������ˮ����������ϡ���ᣬ�ټ���BaCl2��Һ���а�ɫ�������ɡ�
CuSO4+2H2O+SO2��������SO42-һ���������ữ���Ȼ�����Һ����ʵ�鷽����ȡ������ɫ��������ˮ����������ϡ���ᣬ�ټ���BaCl2��Һ���а�ɫ�������ɡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�������A��B��C������ס��ҡ����Լ�����D��E��F��G��H������֮����ת����ϵ����ͼ��ʾ��ͼ����Щ��Ӧ��������ͷ�Ӧ������û�б������

��ش��������⣺
��1��д���������ʵĻ�ѧʽ��B_________����_________����_________��H_________
��2������Ҫ��ش�
1)D��Һ��F��Һ�ڿ����л�ϵ�����_________________________________��
2)��Ӧ�����ӷ���ʽ___________________________________________________��
3)��Ӧ�����ӷ���ʽ___________________________________________________��
4)��Ӧ��ѧ����ʽ___________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10mL 0.1molL��1NaOH��Һ�м���0.1molL��1��һԪ��HA��ҺpH�ı仯������ͼ��ʾ������˵������ȷ���ǣ� �� 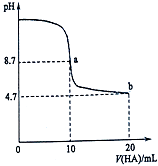
A.����μ���HA��Һ��20mLʱ��NaOH��Һ��ˮ�ĵ���̶���������С
B.b����ʾ��Һ��c��A������c��HA��
C.pH=7ʱ��c��Na+��=c��A����+c��HA��
D.����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ������������ȷ����
A. �ơ������̶��ǽ���
B. �������Һ�ı����������ܷ�������������
C. ���������������ѪҺ�����������˽��������
D. �����ȶ����ڵ���Ҫԭ���ǽ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС���о��������ƣ������������ϣ��Ը�����Ϣ�ش��������⡣
ҩƷ | NaNO2(��������) |
���� | 1.��������Һ���н�ǿ�����ԣ��ܽ�Fe2+������Fe3+�� 2.AgNO2��һ��������ˮ������������Ρ� |
��1����֪NaNO2�ܷ������·�Ӧ:2NaNO2+4HI=2NO��+I2+2NaI+2H2O������˫���ű�ʾ����ת�Ƶķ������Ŀ��________________
�÷�Ӧ����������_____������0.75mol����ת�ƣ���ԭ��������������Ϊ_______��
��2����ʳNaNO2�ᵼ��Ѫ�쵰���е�Fe2+ת��ΪFe3+���ж����ɷ���ά����C�ⶾ�����з����������______(�����)��
A.NaNO2����ԭ B.ά����C���л�ԭ��
C.��ԭ��:ά����C>Fe2+ D.NaNO2�ǻ�ԭ��
��3�������������������NaNO2��NaCl����______ (�����)��
A. ��ɫ��Ӧ B.�ֱ�μ��ữFeSO4��Һ��KSCN��Һ
C.�����������¼���KI������Һ D.�ֱ�μ�AgNO3��Һ
��4��ijͬѧ�����Ƶ���ˮ�ӵ�NaNO2��Һ�У��۲쵽��ˮ��ɫ��ͬʱ����NaNO3��HCl����д����Ӧ�����ӷ���ʽ:_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ο���ͼ���й�Ҫ��ش����⣺ 
��1���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ������һ��ԭ����CH3OH��g����H2O��g����Ӧ����CO2��H2 �� ͼ1�Ǹù����������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ������������Ӧ��� a�ı仯�������������С���������䡱������Ӧ�ȡ�H�ı仯�������������С���������䡱����
��2����CH3OHȼ�ϵ��Ϊ��Դ��ⷨ��ȡClO2 �� �������ȣ�ClO2��Ϊһ�ֻ���ɫ���壬�ǹ����Ϲ��ϵĸ�Ч�����ס����١���ȫ��ɱ���������� ��CH3OHȼ�ϵ�طŵ�����У�ͨ��O2�ĵ缫������Һ��pH�����������С���������䡱����������ӦʽΪ ��
��ͼ2�е�����ʯī���缫����һ�������µ�ⱥ��ʳ��ˮ��ȡ ClO2 �� �������� ClO2�ķ�ӦʽΪ ��
�۵��һ��ʱ�䣬���������ռ�����������������ռ�������� 6.72Lʱ����״�����������ɵ������ܽ⣩��ֹͣ��⣬ͨ�������ӽ���Ĥ��������Ϊmol��
��3��ͼ2�е��ظ�Ϊ��ʯī���缫����һ�������µ��0.05molL��1������ͭ��Һ200mL�����������������������ͬʱ�� �ٷ��������ܷ�Ӧ����ʽΪ
����������Һ���������200mL����Һ��pH=
�۵�����������������ʿ�ʹ��Һ�ָ������ǰ
A CuO B Cu ��OH��2C CuCO3D CuSO4 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���һΪ���ʣ��ڶ�Ϊ���������Ϊ��������
A. ˮ���������������塢Ũ���� B. ʳ�Ρ�����ͭ��Һ������
C. ���ʯ��������������Ư�� D. ����������ʯ����ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У����屻��ԭ����
A. CO2ʹNa2O2���ɫ B. Cl2ʹFeCl2��Һ���ɫ
C. H2ʹ���ȵ�CuO��ĩ���ɫ D. CO2��ʹʯ��ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ����һ��Ԫ�ص�����
A.�����Ǵ�����Ҳ�����ǻ����B.�����ǵ���Ҳ�����ǻ�����
C.һ���Ǵ�����D.һ����һ�ֵ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com