
 һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ��
һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ������ ��1��M���ʵ�������N�����ʵ�����С����NΪ��Ӧ�MΪ���������N�����ʵ��������Ҳ�Ϊ0����÷�Ӧ���ڿ��淴Ӧ���������ʵ���֮�ȵ��ڻ�ѧ������֮��ȷ����ѧ��������������д��Ӧ����ʽ��
��2�����Է�Ӧ����ƽ��״̬ʱ��������������ȣ�����ֵ����ʵ������䣻
��3��t3ʱ��ʱ�������������Ϊ1L����ϵѹǿ������ƽ���ƶ��ķ��������
��4����ѧƽ�ⳣ������������ƽ��Ũ����֮���뷴Ӧ��ƽ��Ũ��Ũ����֮���ı�ֵ��
��5��0-t2 ʱ����ڡ�n��M��=5mol-2mol=3mol������v=$\frac{��n}{V•��t}$���㣻
��6��ͬ��ͬѹ�£���������ʵ���֮�ȵ���ѹǿ֮�ȣ�
��� �⣺��1��M���ʵ�������N�����ʵ�����С����NΪ��Ӧ�MΪ���������N�����ʵ��������Ҳ�Ϊ0����÷�Ӧ���ڿ��淴Ӧ����n��N��=8mol-2mol=6mol����n��M��=5mol-2mol=3mol����N��M�Ļ�ѧ������֮��Ϊ2��1���ʷ�Ӧ����ʽΪ��2N?M��
�ʴ�Ϊ��2N?M��
��2����t2ʱ��M��N�����ʵ���Ϊ��ֵ������ƽ��״̬������t2ʱ��v��=v����
�ʴ�Ϊ��t2��
��3��t3ʱ��ʱ�������������Ϊ1L����ϵѹǿ����ƽ�������ƶ���N�����ʵ�����С����d�����
�ʴ�Ϊ��d��
��4��t2ʱ�̷�Ӧ2N?M����ƽ��״̬����ʱM��ƽ��Ũ��c��M��=$\frac{5mol}{2L}$=2.5mol/L��N��ƽ��Ũ��c��N��=$\frac{2mol}{2L}$=1mol/L����ѧƽ�ⳣ��K=$\frac{c��M��}{{c}^{2}��N��}$=$\frac{2.5}{{1}^{2}}$=2.5��
�ʴ�Ϊ��2.5��
��5��0-t2 ʱ����ڡ�n��M��=5mol-2mol=3mol��V=2L����t=2 min������v��M��=$\frac{��n}{V•��t}$=$\frac{3mol}{2L��2min}$=0.75mol/��L•min����
�ʴ�Ϊ��0.75mol/��L•min����
��6����Ӧǰ��������ʵ���Ϊ8mol+2mol=10mol��ƽ��ʱ��������ʵ���Ϊ2mol+5mol=7mol��ͬ��ͬѹ�£���������ʵ���֮�ȵ���ѹǿ֮�ȣ���˴ﵽƽ��ʱ����ϵ�ڵ�ѹǿ�ǿ�ʼ��$\frac{7mol}{10mol}$=0.7����
�ʴ�Ϊ��0.7��
���� ���⿼�黯ѧƽ����㡢ƽ��״̬��������Ӧ���ʺͻ�ѧƽ�ⳣ��K�����֪ʶ���Ѷ��еȣ�ע���ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ | B�� | Ũ���� | C�� | Ũ���� | D�� | �Ȼ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�78gNa2O2�к��е�����������NA | |
| B�� | m g ${\;}_{Z}^{A}$Xn-��������������Z-n��mNA/A | |
| C�� | 1L0.1mol/LFe��OH��3�����к���Fe��OH��3������Ϊ0.1NA | |
| D�� | H2SO4��Ħ������Ϊ98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 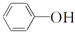 �� ��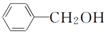 ��ͬϵ�� ��ͬϵ�� | |
| B�� | ����������CH3COOCH2CH3���ĺ˴Ź������׳�������壬�ҷ����֮��Ϊ3��2��3 | |
| C�� | ����ʽΪC4H10���л���һ�ȴ��ﹲ��8�� | |
| D�� | 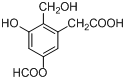 ������������4�� ������������4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʱ�����ƽ������ӵ�Դ����������������Ӧ | |
| B�� | ��ҵ�ϵ��NaClˮ��Һ�Ʊ��ƣ��������̬Al2O3�Ʊ�Al | |
| C�� | ��������բ����ֱ����Դ�ĸ��������������������������������� | |
| D�� | ��⾫��ͭʱ�����Һѡ�������ữ������ͭ�����������У�Cu2+Ũ�Ƚ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{a}{36V}$mol/L | B�� | $\frac{a}{18V}$mol/L | C�� | $\frac{a}{54V}$mol/L | D�� | $\frac{a}{27V}$mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�ۡ����ᡢ��ƺ�Һ�ȶ����ڻ���� | |
| B�� | ����е�1 mol/L NaOH��Һ�еμ�FeCl3������Һ�����Ʊ�Fe��OH��3���� | |
| C�� | �����Ȼ��ƣ������ͭ���ܵ��磬���Զ����ڵ���� | |
| D�� | һ��ƽ�й������䵰������Һʱ���Ӳ�����Կ���һ��������ͨ· |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaB��Һ��pH=8��c��Na+��-c��B-��=9.9��10-6mol•L-1 | |
| B�� | pH��ȵĢ�NH4C1���ڣ�NH4��2SO4����NH4HSO4������Һ�У�c��NH4+����С˳��Ϊ����=�ڣ��� | |
| C�� | Na2CO3��Һ�У�2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | 10mLpH=12������������Һ�м���pH=2��HA��pH�պõ���7��������Һ���V���ܣ���20mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com