
ijС�������֪:������I >Fe3+>I2,3Br2+6FeCl2
>Fe3+>I2,3Br2+6FeCl2 2FeBr3+4FeCl3;I2+2S2
2FeBr3+4FeCl3;I2+2S2
 S4
S4 +2I-;CuI��һ�ְ�ɫ����(Ksp=1.3��1
+2I-;CuI��һ�ְ�ɫ����(Ksp=1.3��1 )��
)��
��.��С��Ϊȷ��һ�ݼӵ���(���ܺ���KIO3��KI��Mg2+��Fe3+)�ijɷ�,��ƶ���ʵ����Բ������֤��
(1)ʵ���������:
ʵ�鲽�� | ʵ����̺����� | ��Ӧ���� | |
����1 | ȡһ��������,����������ˮ�ܽ�,����ϡ�����ữ,��������Һ��Ϊ3�� |
_____________ | |
�� �� 2 | ������ ��Һ |
| �����п϶����������� |
������ ��Һ |
|
_____________ | |
������ ��Һ |
| XΪ������(�ѧʽ) | |
(2)�õ����п϶���������������������(�û�ѧʽ�����ӷ��ű���)��
(3)������Ϣ�ƶ�Fe3+��S4 ��I2��Br2����������ǿ������˳������������������������
��I2��Br2����������ǿ������˳������������������������
(4)��������Һ�м�������KI�����,��Ӧ�����ӷ���ʽΪ��������������������������������������
��.������ӵ��������ⶨ����CuCl2��2H2O���������(��������I-������Ӧ������������)�Ĵ���,��������:
ȡ0.40 g��������ˮ,�������KI����,��ַ�Ӧ,���ɰ�ɫ����������������ζ�ָʾ��,��0.100 0 mol��L-1 Na2S2O3����Һ�ζ�,����ζ��յ�ʱ,����Na2S2O3����Һ20.00 mL��
(1)�ζ��յ������������
(2)CuCl2��Һ��KI��Ӧ�Ļ�ѧ����ʽΪ��������������������������������
(3)��������CuCl2��2H2O��������������������
��.(1)Fe3+��CCl4��(2)KI
(3)Br2>Fe3+>I2>S4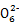
(4)2Fe3++2I- 2Fe2++I2,I
2Fe2++I2,I +5I-+6H+
+5I-+6H+ 3I2+3H2O
3I2+3H2O
��.(1)��ɫ��ȥ,����һ��ʱ��ָ�ԭɫ(����������ɫ���仯)
(2)2CuCl2+4KI 2CuI��+I2+4KCl
2CuI��+I2+4KCl
(3)85.5%
����������.(2)�ɲ����ڢ���֪��Һ��һ������KI,��ϼӵ�ʳ�ο�֪һ������KIO3;(4)��Һ�е�Fe3+��I ����I-��Ӧ;��.����2CuCl2+4KI
����I-��Ӧ;��.����2CuCl2+4KI 2CuI��+I2+4KCl��I2+2S2
2CuI��+I2+4KCl��I2+2S2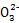
 S4
S4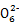 +2I-��֪CuCl2~S2
+2I-��֪CuCl2~S2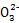 ,n(CuCl2)=n(S2
,n(CuCl2)=n(S2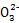 )=2��10-3 mol,m(CuCl2��2H2O)=0.342 g
)=2��10-3 mol,m(CuCl2��2H2O)=0.342 g


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ���ָ�ϰ ר��10�����ǽ���Ԫ�ؼ�����Ҫ��������ϰ���������棩 ���ͣ�ʵ����
SiO2��SO2��CO2����������������ǵĻ�ѧ���ʾ���һ���������ԣ�Mg��Na�Ļ�ѧ����Ҳ����һ�������ԡ�
ij��ȤС������ͼ��ʾװ�ý���Mg��SO2��Ӧ��ʵ�顣

(1)ѡ����ȡSO2�ĺ����Լ�________(����)��
��ŨHCl����ŨH2SO4����Na2SO3���塡��CaSO3����
(2)����װ�û����Ż����Ż��ķ�����________________________________________��װ��C��NaOH��Һ��������___________________________________________________________
(3)��ͬѧ�Ʋ�Mg��SO2�ķ�Ӧ��Mg��CO2�ķ�Ӧ���ƣ���÷�Ӧ����ʽΪ_________________________________________��
��ͬѧ���Ʋ��ǣ�2Mg��3SO2 2MgSO3��S����ͬѧ���Ʋ��ǣ�3Mg��SO2
2MgSO3��S����ͬѧ���Ʋ��ǣ�3Mg��SO2 2MgO��MgS��Ҫ��֤�ס��ҡ�����λͬѧ���Ʋ��Ƿ���ȷ����ͬѧ������ʵ��̽����
2MgO��MgS��Ҫ��֤�ס��ҡ�����λͬѧ���Ʋ��Ƿ���ȷ����ͬѧ������ʵ��̽����
��֪��MgSO3��MgS������ˮ���������ᷢ�����ֽⷴӦ�ų����壻H2S����ͨ��CuSO4��Һ�г��ֺ�ɫ������
��ѡ�Լ���2 mol��L��1���ᡢ2 mol��L��1���ᡢ����ˮ��2 mol��L��1 NaOH��Һ��Ʒ����Һ������ʯ��ˮ��2 mol��L��1 CuSO4��Һ����������Ʒ��ѡ��
��� | ʵ�鲽�� | Ԥ������ͽ��� |
�� | ȡ������Ӧ�����ù������Թ��� |
|
�� | ���Թ��еĹ��������μ�____________���Թܿ����ϴ����ܵĵ���������������ͨ��ʢ��________���Թ��� | ���Թ��е�________�����ͬѧ�Ʋ���ȷ�����Թ��еĹ���δ��ȫ�ܽ⣬��________������ͬѧ�Ʋ���ȷ |
��������ʵ��̽������֤����ͬѧ�Ʋ���ȷ�IJ�����Ԥ��������
_____________________________________________________________��
(4)����ʵ����Ҫ100 mL 2 mol��L��1�����ᣬ����ʱѡ��________(ѡ��10 mL��25 mL��50 mL��100 mL)��Ͳ��ȡ36.5%�ܶ�Ϊ1.19 g��mL��1��Ũ��������Ϊ________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ���ֳ�̷�ѡ��������ר�� ��ѧ����������ϰ���������棩 ���ͣ������
��ҵ̼����(����ԼΪ98%)�к���Ca2����Mg2����Fe3����Cl����SO42�������ʣ��ᴿ�����������£�

��.̼���Ƶı�����Һ�ڲ�ͬ�¶�����������������ͼ��ʾ��

��.�й����ʵ��ܶȻ����£�
���� | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
Ksp | 4.96��10��9 | 6.82��10��6 | 4.68��10��6 | 5.61��10��12 | 2.64��10��39 |
�ش��������⣺
(1)����NaOH��Һ����˵õ�����������Ҫ����________(��д��ѧʽ)��25��ʱ������Mg2����Fe3������Һ�еμ�NaOH��Һ�������ֳ�����������Һ��pH��8 ʱ��c(Mg2��)��c(Fe3��)��________��
(2)����XΪ________�����¶�Ӧ������_____________________________________
(3)���˴�����ɫ��ѧ���Ƕ����뽫��ĸҺ����������������ʾ����ѭ��ʹ�á��������ʵ�ʹ�ҵ�������Ƿ����________����˵������______________________________
________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ���ֳ��ѡ������ʱ����ר�� ����������ϰ���������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ�����з�˵����ȷ����(����)
A��25 ��ʱ��pH��13��1.0 L Ba(OH)2��Һ�к��е�OH����ĿΪ0.2 NA
B����״���£�2.24 L Cl2��������H2O��Ӧ��ת�Ƶĵ�������Ϊ0.1 NA
C����״���£�22.4 L�״�(CH3OH)�к��е���ԭ����Ϊ1.0 NA
D��4.6 g Na�ڿ�������ȫ��Ӧ����Na2O��Na2O2��ת��0.2 NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ����ר�⸴ϰ���ʵ���ɷ��༰�����仯��ϰ���������棩 ���ͣ�ѡ����
��200 mLij��������Һ��,����1.5NA����������� (NA��ʾ�����ӵ�������ֵ),ͬʱ����NA���������ӡ���������ε����ʵ���Ũ��Ϊ(����)
A.2 mol��L-1B.2.5 mol��L-1C.5 mol��L-1D.7.5 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ����ר�⸴ϰ ���ӷ�Ӧ��������ԭ��Ӧ��ϰ���������棩 ���ͣ�ѡ����
ijͬѧ��������Ӧ��Ӧ�����ӷ���ʽ����������,���к�������(����)
ѡ����ѧ��Ӧ���ӷ���ʽ����
A̼�����Ƶ�ˮ��HC +H2O
+H2O H3O++C
H3O++C ��ȷ
��ȷ
BNaHCO3��Һ�е���NaOH��ҺHC +OH-
+OH- CO2��+H2O����,��ɲ��غ�
CO2��+H2O����,��ɲ��غ�
C��84����Һ��(��Ч�ɷ�ΪNaClO��Һ)�����������(��Ч�ɷ�ΪŨ����)��Ϸų�����ClO-+Cl-+H+ Cl2��+OH- ��ȷ
Cl2��+OH- ��ȷ
D������FeBr2�����Cl2��Ӧ2Fe2++2Br-+2Cl2 2Fe3++Br2+4Cl- ����,Fe2+��Br-�����ʵ���֮���뻯ѧʽ����
2Fe3++Br2+4Cl- ����,Fe2+��Br-�����ʵ���֮���뻯ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ����ר�⸴ϰ �������Һ�����ƽ����ϰ���������棩 ���ͣ������
pC����pH,��ָ��ϡ��Һ��,�������ʵ���Ũ�ȵij��ö�����ֵ����ij��Һ���ʵ�Ũ��Ϊ1��10-3mol��L-1,�����Һ�����ʵ�pC=-lg(1��10-3)=3����ͼΪ,H2CO3�ڼ���ǿ���ǿ����Һ��,ƽ��ʱ��Һ�����ֳɷֵ�pC��pHͼ����ش���������:

(1)������ѪҺ��,HC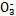 ����ʹ����ѪҺpH������7.35~7.45�����á������õ������Һ�е�ƽ�����:������������������������������(�����ӷ���ʽ��ʾ)��
����ʹ����ѪҺpH������7.35~7.45�����á������õ������Һ�е�ƽ�����:������������������������������(�����ӷ���ʽ��ʾ)��
����������ѪҺ��,HC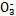 ��ˮ��̶�������������̶�(����<����>������=��)��
��ˮ��̶�������������̶�(����<����>������=��)��
��pH=7.00��ѪҺ��,c(H2CO3)��������c(HC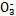 )(����<����>������=��)��
)(����<����>������=��)��
(2)H2CO3һ������ƽ�ⳣ������ֵ ������������
������������
(3)ijͬѧ��Ϊ����Һ��Na2CO3��ˮ��������,����ˮ���C ��������������10%��������Ƽ�ʵ��֤����ͬѧ�Ĺ۵��Ƿ���ȷ
��������������10%��������Ƽ�ʵ��֤����ͬѧ�Ĺ۵��Ƿ���ȷ
����
(4)��֪ij�¶���Li2CO3��KspΪ1.68��10-3,������Li2CO3��������100 mLˮ�����պñ���,����Li2CO3��Һ��c(Li+)=0.15 mol��L-1��c(C )=0.075 mol��L-1����t1ʱ����������ϵ�м���100 mL 0.125 mol��L-1 Na2CO3��Һ,��ʽ����˵���Ƿ��г���������
)=0.075 mol��L-1����t1ʱ����������ϵ�м���100 mL 0.125 mol��L-1 Na2CO3��Һ,��ʽ����˵���Ƿ��г���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��߿���ѧ����ר�⸴ϰ �绯ѧ��ϰ���������棩 ���ͣ�ѡ����
��������˵������ȷ����(����)
A.�ö��Ե缫��������Ȼ��Ƶ����ӷ���ʽΪ:2Cl-+2H2O Cl2��+H2��+2OH-
Cl2��+H2��+2OH-
B.�ö��Ե缫�ֱ���CuCl2��Һ��MgCl2��Һ�ֱ�õ�����Cu��Mg
C.��ͼΪ��������Ȼ�����Һ��װ��,һ��ʱ��������ռ�����������֮��Ϊ1��1

D.��⾫��ͭʱ,��ͬʱ������������ͭ�������������ܽ�ͭ��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com