
【题目】铁铝合金8.3g溶于300mL2mol/L盐酸时,在标准状况下产生气体5.6L。若向反应后的溶液中加入适量烧碱溶液,充分搅拌,生成沉淀的最大质量为
A. 9g B. 16.8g C. 18.5g D. 22.5g
【答案】C
【解析】发生反应Fe+2HCl=FeCl2+H2↑,2Al+6HCl=2AlCl3+3H2↑,5.6L气体是氢气,氢气的物质的量为![]() =0.25mol,故参加反应的HCl的物质的量为0.25mol×2=0.5mol,溶液中n(HCl)=0.3L×2mol/L=0.6mol,大于参加反应的HCl的物质的量,故金属完全反应,反应后溶液中加入适量烧碱溶液,充分搅拌,生成沉淀的质量最大,则亚铁离子(搅拌过程被氧化为铁离子)、铝离子恰好完全转化为Fe(OH)3、Al(OH)3,则m(沉淀)=m(金属)+m(OH-),根据电子得失守恒及考虑亚铁离子氧化,若假设金属全部为铝,可知最终增加的n(OH-)=2n(H2)=0.25mol×2=0.5mol,故沉淀的最大质量为8.3g +0.5mol×17g/mol=16.8g;若假设金属全部为铁,可知最终增加的n(OH-)=2n(H2)×
=0.25mol,故参加反应的HCl的物质的量为0.25mol×2=0.5mol,溶液中n(HCl)=0.3L×2mol/L=0.6mol,大于参加反应的HCl的物质的量,故金属完全反应,反应后溶液中加入适量烧碱溶液,充分搅拌,生成沉淀的质量最大,则亚铁离子(搅拌过程被氧化为铁离子)、铝离子恰好完全转化为Fe(OH)3、Al(OH)3,则m(沉淀)=m(金属)+m(OH-),根据电子得失守恒及考虑亚铁离子氧化,若假设金属全部为铝,可知最终增加的n(OH-)=2n(H2)=0.25mol×2=0.5mol,故沉淀的最大质量为8.3g +0.5mol×17g/mol=16.8g;若假设金属全部为铁,可知最终增加的n(OH-)=2n(H2)×![]() =0.25mol×2×
=0.25mol×2×![]() =0.75mol,故沉淀的最大质量为8.3g +0.75mol×17g/mol=21.05g,故生成沉淀最大质量应大于16.8g,小于21.05g,答案选C。
=0.75mol,故沉淀的最大质量为8.3g +0.75mol×17g/mol=21.05g,故生成沉淀最大质量应大于16.8g,小于21.05g,答案选C。


科目:高中化学 来源: 题型:
【题目】水体中重金属铅的污染问题备受关注。查资料知Pb4+具有很强的氧化性,水中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2( 在水中溶解度小)、Pb(OH)3-、Pb(OH)42-,各形态的物质的量分数a随溶液pH变化的关系如下图所示:
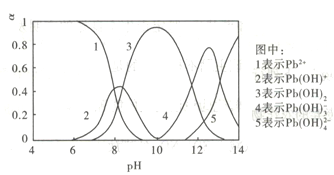
下列有关说法正确的是
A. Pb(NO3)2溶液中,c(Pb2+)/c(NO3-)=1/2
B. 向Pb(NO3)2波中滴加氯化铵溶液,溶液中c(Pb2+)/c(NO3-)变小,可能是Cl-与Pb2+发生反应
C. 向Pb(NO3)2溶液中滴加NaOH溶液,pH 越大,生成沉淀越多
D. pH=12时,混合体系中发生的主要反应的离子方程式为Pb(OH)3-+OH-=Pb(OH)42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素性质对比正确的是
A. 金属性:K>Na>Cs B. 稳定性:SiH4>H2S>HCl
C. 酸性:H2CO3>H2SiO3>HClO4 D. 非金属性:Cl>S>P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于A2+3B2═2C+D(均为气态物质)的反应来说,以下化学反应速的表示中,反应速率最快的是( )
A.v(A2)=0.4 molL﹣1s﹣1
B.v(D)=6 molL﹣1min﹣1
C.v(C)=0.6 molL﹣1s﹣1
D.v(B2)=0.8 molL﹣1s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)![]() nY(g) ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积(容器容积)的关系如下表所示:
nY(g) ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积(容器容积)的关系如下表所示:
气体体积/L | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《中华人民共和国大气污染防治法》于2016年1月1日起实施。为保护和改善大气环境,下列做法不应该提倡的是
A. 开发生物质能替代化石燃料 B. 向高空排放金属冶炼产生的粉尘
C. 用催化转化技术处理汽车尾气 D. 大力推广生产和使用无氟冰箱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列各问题:
(1)①泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:__________;
②TiCl4水解生成TiO2·xH2O的化学方程式__________;
③酸性高锰酸钾溶液与草酸溶液反应的化学方程式____________;
④硫代硫酸钠溶液与稀硫酸反应的化学万式____________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出
①电荷数守恒_________;
②物料守恒___________;
③质子守恒___________;
④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)_________。
(3)常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。所用NaOH溶液浓度为____________。
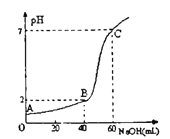
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对 ![]() X与
X与 ![]() X+两种微粒,下列叙述正确的是( )
X+两种微粒,下列叙述正确的是( )
A.一定都是由质子、中子、电子组成的
B.质子数一定相同,质量数和中子数一定不相同
C.核电荷数和核外电子数一定相等
D.化学性质几乎完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com