
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
| A.合金的熔点一般比组分金属低 |
| B.铝钠合金若投入一定量的水中可得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |
D
解析试题分析:A.合金是由金属与金属或金属与非金属融合而成的具有金属性质的物质。合金具有许多良好的物理的、化学的或机械加工方面的性能,一般熔点比成分金属低,硬度比成分金属高。铝钠合金呈液体,证明它的熔点比成分金属低。正确。B.铝钠合金若投入一定量的水中发生反应2:Na+2H2O=2NaOH+H2↑.2NaOH+2Al+2H2O=2NaAlO2+3H2↑.可见只要n(Al)≤n(Na),就可得到无色溶液。正确。C.铝钠合金投入到足量氯化铜溶液中,Na和水反应产生氢氧化钠和氢气,氢氧化钠与氯化铜溶液发生复分解反应达到氢氧化铜程度;也可能是铝与氯化铜反应置换反应产生铜和氯化铝。故可能会有氢氧化铜沉淀也可能有铜析出。正确。D.2Al+6HCl=AlCl3+3H2↑.2Na+2HCl="2NaCl+" H2↑.可见产生相等质量的氢气,需要的金属钠的质量要多。即等质量的铝和钠,铝反应放出的H2多。因此,若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越大。错误。
考点:考查Na、Al的化学性质。


科目:高中化学 来源: 题型:单选题
下列有关金属铝及其化合物的叙述正确的是
| A.铝在常温下不能与氧气反应 | B.铝不能与氯气反应 |
| C.氧化铝只能与酸反应,不能与碱反应 | D.铝既能溶于酸,又能溶于强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
| A.取a克混合物充分加热,得b克固体 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。 |
| D.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将1 L 1.00 mol/L 的Na2CO3溶液逐滴加入到1 L 1.25 mol/L的盐酸中;再做相反操作:将1 L 1.25 mol/L的盐酸逐滴加入1 L 1.00 mol/L 的Na2CO3溶液中,两次操作产生的气体体积之比(同温同压下)是:( )
| A.1∶1 | B.2∶1 | C.5∶2 | D.2∶5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
取16.8g碳酸氢钠固体,加热一段时间后,剩余固体的质量为13.7g。把剩余固体加入到100mL 2mol/L的稀硫酸中,充分反应后溶液中H+的浓度约为
| A.3 mol/L | B.2 mol/L | C.1.4 mol/L | D.1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知室温下,Al(OH)3的Ksp远大于Fe(OH)3。向浓度均为0.1mol/L的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积关系,合理的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,A、B中分别有10 mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )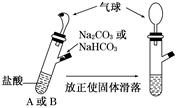
A.A装置的气球膨胀速率大
B.若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L
C.若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L
D.最终两试管中Na+、Cl-的物质的量一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法不正确的是( )
| A.干燥的氯气可以用钢瓶运输 |
| B.钠可以保存在CCl4液体中(已知:密度CCl4 > Na) |
| C.Na2O2可作为潜水艇的供氧剂 |
| D.实验后剩余的钠粒可放回原试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com