

| A.通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等 |
| B.将卤水中Mg2+转化为氢氧化镁沉淀通常是向卤水加入氢氧化钠溶液 |
| C.直接加热MgCl2·6H2O可得到较纯净的无水MgCl2 |
| D.在高温下用铝还原MgCl2可制取金属镁 |
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源:不详 题型:填空题

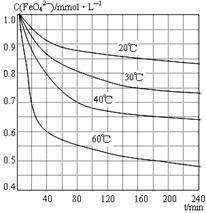
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
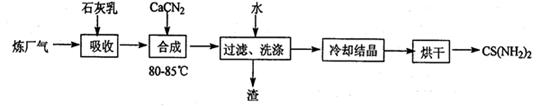
 2H2(g)+S2(g),其平衡常数表达式为K=。
2H2(g)+S2(g),其平衡常数表达式为K=。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.充分利用太阳能 |
| B.因地制宜开发利用风能、水能、地热能、潮汐能 |
| C.合理、安全开发利用氢能、核能 |
| D.能源都是通过化学反应获得的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.利用太阳能,将海水蒸馏淡化 |
| B.加入明矾,使海水的盐份沉淀并淡化 |
| C.通直流电,采用电渗透法使海水淡化 |
| D.通过离子交换膜,除去所含的盐分使海水淡化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇汽油是一种纯净物 |
| B.乙醇汽油作燃料不会产生碳氧化物等有害气体,其优点是可以减少对环境的污染 |
| C.乙醇和汽油都可作溶剂,也可相互溶解 |
| D.乙醇和乙二醇互为同系物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
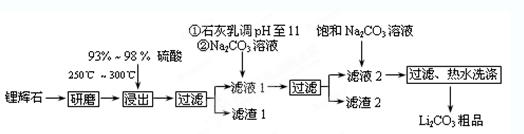
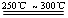 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com