
| A. | NH3、HD、CH4 | B. | HCl、CO2、H2SO4 | C. | SO2、SiO2、P2O5 | D. | CCl4、Na2S、H2O |
分析 化合物由两种或两种以上的元素组成的纯净物.分子间通过分子间作用力(包括范德华力和氢键)构成的晶体.常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等.
解答 解:A、NH3、CH4于分子晶体的化合物,HD是单质,不是化合物,故A错误;
B、HCl,CO2,H2SO4属于分子晶体的化合物,故B正确;
C、SO2、P2O5属于分子晶体的化合物,SiO2为原子晶体,不是分子晶体,故C错误;
D、CCl4、H2O属于分子晶体的化合物,Na2S是离子晶体,不是分子晶体,故D错误.
故选:B.
点评 考查常见物质晶体类型判断等,难度不大,掌握常见物质晶体类型及常见分子晶体.


科目:高中化学 来源: 题型:选择题
| A. | a=b | B. | a<b | C. | b=10-4a | D. | a=10-4b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4(s)?Ba2+(aq)+SO42- (aq) | B. | HClO═H++ClO- | ||
| C. | NaHSO4?Na++H++SO42- | D. | H2S?H++HS-、HS-?H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯环的碳碳键键长都相等 | |
| B. | 苯分子中有C=C,所以能使溴水反应而褪色 | |
| C. | 邻-二溴苯没有同分异构体 | |
| D. | 常温下苯是一种不溶于水且密度小于水的液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、O=C=O.
、O=C=O.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
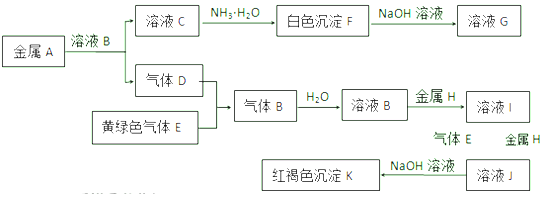
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com