
【题目】下列属于非电解质的是
A.氯化钠B.氨气C.氯水D.铜
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:
【题目】化学实验的基本操作是完成化学实验的关键,下列实验操作正确的是( )
①用50 mL量筒量取5.2 mL稀硫酸; ②用分液漏斗分离苯和四氯化碳的混合物;
③用托盘天平称量117.7 g氯化钠晶体; ④用量筒量取23.10 mL溴水;
⑤用蒸发皿高温灼烧石灰石; ⑥用250 mL容量瓶配制250 mL 0.2 mol·L-1的NaOH溶液;
A. ③⑥ B. ②③④⑤ C. ①②④ D. ②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种蔗糖燃料电池的装置如图所示,下列说法正确的是
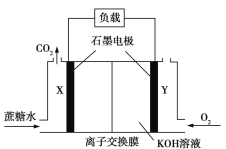
A.Y电极附近溶液pH减小
B.右室的K+移向左室
C.X电极的电极反应式为:C12H22O1136e+13H2O![]() 12CO2↑+48H+
12CO2↑+48H+
D.理论上电池工作时X电极生成的气体与Y电极消耗的气体物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示:
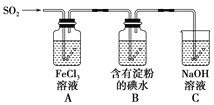
(1)A装置中发生反应的离子方程式为_________________________________________。
(2)B装置中发生反应的离子方程式为_________________________________________。
(3)下列实验方案适用于在实验室制取所需SO2的是________。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(4)装置C的作用是__________________________________________________。
(5)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有________(填序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(6)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是________,原因是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下:

(1)A的分子式是C7H8,其结构简式是________________________。
(2)试剂a是____________________。
(3)反应③的化学方程式:_________________________________________________。
(4)E的分子式是C6H10O2。E中含有的官能团:_________________________。
(5)反应④的反应类型是____________________________。
(6)反应⑤的化学方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的说法中不正确的是 ( )
A. 化学键是一种作用力
B. 化学键可以使原子相结合,也可以使离子相结合
C. 化学反应过程中,反应物分子内的化学键断裂,产物分子中的化学键形成
D. 非极性键不是化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关晶体的说法中正确的是( )
A. 氯化钾溶于水时离子键未被破坏 B. 原子晶体中共价键越强,熔点越高
C. 晶体中有阳离子必含阴离子 D. 分子间作用力越大,分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有标准状况下V L 气体AB3,它的摩尔质量为M g·mol-1。则:
(1)该气体所含原子总数为________________个(列出计算式即可,下同)。
(2)该气体的质量为_____________g。
(3)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______________。
(4)该气体溶于水后形成1 L溶液,其溶液的物质的量浓度为_______________ mol·L-1。
(5)该气体溶于1L水中(不考虑反应),若所得溶液的密度为ρg·mL-1,则溶液的物质的量浓度为_____________________mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1) 元素M的核外电子排布式________ ;元素L的电子排布图为________ ;
(2)五种元素的原子半径从大到小的顺序是____________(用元素符号表示)。Y、Z、L的电离能由大到小的顺序是______________(用元素符号表示)
(3)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的分子空间构型为__________,中心原子的杂化方式是________,A的电子式为____________,B的结构式为____________。
(4)NO3-的空间构型为__________;写出NO3-互为等电子体的一种分子的化学式_____________。
(5)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为____,每个Ba2+与__个O2-配位。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com