
【题目】某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是

A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
【答案】C
【解析】由图象分析可知,开始无沉淀生成说明加入的盐酸和溶液中的碱反应,说明溶液中一定含OH-离子,则与氢氧根离子不能共存的是Fe3+、Mg2+、Al3+;随后反应生成沉淀逐渐增大,说明是AlO2-、SiO32-和氢离子反应生成氢氧化铝沉淀和硅酸沉淀,由于AlO2-与HCO3-发生反应生成氢氧化铝沉淀,则溶液中一定不存在HCO3-;继续加入盐酸沉淀量不变,消耗盐酸的离子只能是CO32-离子,反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐酸,最后剩余沉淀为硅酸;硫酸根离子不能确定是否存在,但根据溶液的电中性可知,溶液中一定含有Na+离子。A.溶液中硫酸根离子不能确定,剩余原溶液中不一定含有Na2SO4,故A错误;B.依据判断原溶液中一定含有的阴离子是:OH-、SiO32-、AlO2-、CO32-,故B错误;C.依据图像可知和碳酸根离子反应的盐酸为2体积,CO32-+2H+=CO2↑+H2O 氢氧化铝溶解消耗的盐酸体积为4体积,Al(OH)3+3H+=Al3++3H2O,原溶液中含有CO32-与AlO2-的物质的量之比为3:4,故C正确;D.根据图像溶解氢氧化铝消耗的盐酸体积为4,假设盐酸的浓度为1mol/L,则消耗氯化氢4mol,则溶解的氢氧化铝为![]() mol,则溶液中含有
mol,则溶液中含有![]() mol AlO2-,沉淀
mol AlO2-,沉淀![]() mol AlO2-需要盐酸
mol AlO2-需要盐酸![]() mol,a-d对应于AlO2-和SiO32-消耗的盐酸大于
mol,a-d对应于AlO2-和SiO32-消耗的盐酸大于![]() mol,即a-d>
mol,即a-d>![]() ,故D错误;故选C。
,故D错误;故选C。


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.运用已学知识完成下列计算:
(1)0.5 mol CH4的质量是________,在标准状况下的体积为________。
(2)3.1 g Na2X含有Na+ 0.1 mol,则X的相对原子质量为________。
Ⅱ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O
(1)该反应中,氧化剂是________,氧化产物是_____。
(2)当有3mol I2生成时,有______mol还原剂被氧化。
(3)用双线桥表示该反应电子转移的方向和数目_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是________(填序号,下同),属于电解质的是_______。
(2)向④中逐滴滴加⑦,可观察到的现象是_______________________。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(1)右图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是__________(填字母)。

(2)有同学认为所有酸碱中和反应均可表示为:H+ + OH = H2O。请举个例子反驳上述观点(用离子方程式表示)______________________________________。
(3)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是:4Ag+2H2S+O2 = 2X+2H2O。则 X的化学式为_______。其中H2S是该反应的_______(填序号)。
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,其在电解质储罐和电池间不断循环。下列说法不正确的是
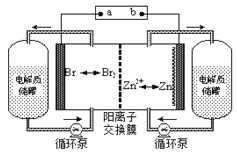
A. 放电时负极的电极反应式为Zn-2e-=Zn2+
B. 充电时电极a为电源的负极
C. 阳离子交换膜可阻止Br2与Zn直接发生反应
D. 放电时左侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是

A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组实验室模拟工业制备硫氰化钾(KSCN)。实验装置如图:
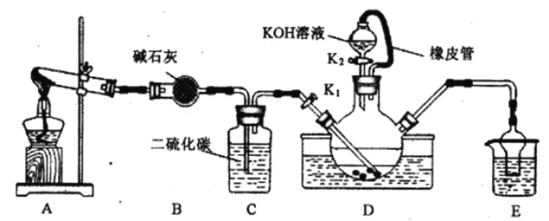
实验步骤如下:
(1)制备 NH4SCN溶液:CS2+2NH3![]() NH4SCN+H2S。该反应比较缓慢。
NH4SCN+H2S。该反应比较缓慢。
①实验前,应进行的操作是______________________。三颈烧瓶内盛放有CS2、水和催化剂,三颈烧瓶的下层CS2液体必须浸没导气管口,目的是______________________。
②实验开始时打开K1,加热装置A、D,缓缓地向装置D中充入气体。装置A中的物质是___________(以化学式表示),装置C的作用可能是______________________。
(2)制备KSCN溶液:移去A处的酒精灯,关闭K1,打开K2,利用耐碱分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是_________________________________。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,___________,过滤,干燥,得到硫氰化钾晶体。
(4)测定KSCN的含量称取10.0g样品配成1000mL溶液量取20.00mL于锥形瓶中,并加入几滴Fe(NO3)3溶液,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消AgNO3标准溶液20.00mL。
①滴定时发生的离子反应为SCN-+Ag+= AgSCN↓,则终点时的现象是___________。
②KSCN的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是
A. 18.0 g淀粉[(C6H10O5)n]和葡萄糖混合物中共含碳原子数为0.6 NA
B. 标准状况下,22.4 L己烷含有的分子数为NA
C. 14g聚乙烯含有的碳原子数目为NA
D. 1 mol 羟基中含有的电子数10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将1.92gCu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL的NOX混合气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入标准状况下的O2的体积为( )
A. 504mLB. 336mLC. 224mLD. 168mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生活中应用广泛。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集的气体体积均小于2.24 L(标准状况),最主要的原因是____________________________;所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因:________________________________。
(2)氧化铁是重要的工业颜料,下面是制备氧化铁的一种方法(铁屑表面常附着油污),其流程如下:
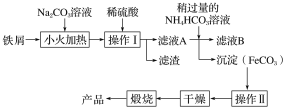
①操作Ⅰ的名称是________;操作Ⅱ为洗涤,洗涤操作的具体方法为__________________。
②滤液A中加入稍过量的NH4HCO3溶液,生成沉淀的同时有一种气体(能使澄清石灰水变浑浊)产生,写出其化学方程式: __________________________________。
(3)如果煅烧不充分,产品中将有FeO存在,称取3.0 g氧化铁产品,加酸溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中,用酸化的0.010 00 mol·L-1 KMnO4溶液滴定至终点,重复滴定2~3次,消耗酸性KMnO4溶液体积的平均值为20.00 mL。
①该实验中的KMnO4溶液需要酸化,用于酸化的酸是________(填序号)。
a.硝酸 b.盐酸 c.硫酸
②上述产品中Fe2O3的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com