
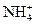 、Ca2+等,进行以下实验(所加酸、碱、氨水、溴水都是过量的)。
、Ca2+等,进行以下实验(所加酸、碱、氨水、溴水都是过量的)。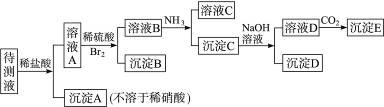
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.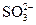 :先加BaCl2溶液,再加稀硝酸,有沉淀生成 :先加BaCl2溶液,再加稀硝酸,有沉淀生成 |
| B.Cl-:先加稀盐酸酸化,再加AgNO3有白色沉淀生成 |
C.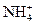 :加浓NaOH溶液共热,有能使湿润的红色石蕊试纸变蓝的刺激性气味气体生成 :加浓NaOH溶液共热,有能使湿润的红色石蕊试纸变蓝的刺激性气味气体生成 |
| D.Fe2+:加氯水,再加KSCN溶液显血红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
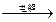 Z+P+Q;②Z+Q
Z+P+Q;②Z+Q X+H+Y。请针对以下两种不同情况来完成:
X+H+Y。请针对以下两种不同情况来完成:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH溶液 | B.氨水 | C.Ba(OH)2溶液 | D.AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.焰色反应是金属元素单质的性质 |
| B.矿泉水含微量锌、钙、镁“元素” |
| C.质谱仪用于测定物质的相对分子质量 |
| D.红外光谱和核磁共振谱反映了物质的结构特点 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同位素:金刚石、石墨 | B.非极性分子:H2O、NH3 |
C.同系物: -OH、 -OH、 -CH2OH -CH2OH | D.同分异构体:HCOOCH3、HOCH2CHO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.25℃时,MgCO3饱和溶液中c(Mg2+)=2.6×10-3mol·L-1,CaCO3饱和溶液中c(Ca2+)=5.3×10-5mol·L-1,向浓度均为0.1 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入0.1 mol·L-1的Na2CO3溶液,首先生成 CaCO3沉淀 |
| B.向硫酸亚铁溶液中加入氯水,再加入KSCN溶液,溶液变为红色,说明硫酸吼i铁溶液中存存Fe3+ |
| C.向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42- |
| D.除去Cu粉中混有的CuO,可将混合物加入到稀硝酸中,充分反应后过滤、洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com