
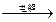 Z+P+Q;②Z+Q
Z+P+Q;②Z+Q X+H+Y。请针对以下两种不同情况来完成:
X+H+Y。请针对以下两种不同情况来完成: ;2H++2e-=H2↑;Cl2+2OH-====Cl-+ClO-+H2O
;2H++2e-=H2↑;Cl2+2OH-====Cl-+ClO-+H2O

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:不详 题型:实验题
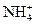 、Ca2+等,进行以下实验(所加酸、碱、氨水、溴水都是过量的)。
、Ca2+等,进行以下实验(所加酸、碱、氨水、溴水都是过量的)。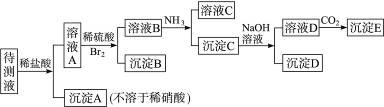
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无论乙烯与丙烯酸以何种比例混合,只要二者总物质的量是个定值,完全燃烧时所 消耗的氧气也一定是个定值 |
| B.鉴别甲苯、苯乙烯、苯酚、丙烯酸溶液可选用KMnO4溶液、溴水 |
| C.可以利用燃烧法来区别聚乙烯塑料和聚氯乙烯塑料、毛和棉 |
| D.装溴水、高锰酸钾溶液的试剂瓶不能用橡胶塞,因为橡胶分子中含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定存在NO2、Br2、HCl | B.一定不存在Br2、NH3、CH4 |
| C.一定存在NO2、HCl、CO2 | D.可能存在NH3、CH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.互溶的液体混合物可以用分液的方法进行分离 |
| B.互不相溶的液体混合物可以用分液的方法进行分离 |
| C.沸点不同的混合物可以用蒸馏的方法进行分离 |
| D.可溶于水的固体与难溶于水的固体的混合物可用溶解、过滤的方法进行分离 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 实验操作 | 实验现象 |
| 步骤1 | 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份 | 有少量气泡产生,溶液的黄绿色褪去 |
| 步骤2 | 将第一份滤液与稀盐酸混合 | 产生大量气泡 |
| 步骤3 | 将第二份滤液加热 | 溶液变浑浊,且有大量无色气体产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除去溴化钠溶液中含有的碘化钠:加入氯水充分振荡后,再加四氯化碳,萃取分液 |
| B.用结晶法提纯NaC和KNO3的混合物中的KNO3 |
| C.用蒸馏法分离汽油和柴油混合物 |
| D.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com