
【题目】(14分)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题.
Ⅰ.H2S的除去
方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3═S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 ![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是 .
(2)由图1和图2判断使用硫杆菌的最佳条件为 . 若反应温度过高,反应速率下降,其原因是 . 
(3)方法2:在一定条件下,用H2O2氧化H2S
随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同.当n(H2O2)/n(H2S)=4时,氧化产物的分子式为 .
(4)Ⅱ.SO2的除去
方法1(双碱法):用NaOH吸收SO2 , 并用CaO使NaOH再生
NaOH溶液 ![]() Na2SO3溶液
Na2SO3溶液
写出过程①的离子方程式:;CaO在水中存在如下转化:
CaO(s)+H2O (l)═Ca(OH)2(s)Ca2+(aq)+2OH﹣(aq)
从平衡移动的角度,简述过程②NaOH再生的原理 .
(5)方法2:用氨水除去SO2
已知25℃,NH3H2O的Kb=1.8×10﹣5 , H2SO3的Ka1=1.3×10﹣2 , Ka2=6.2×10﹣8 . 若氨水的浓度为2.0molL﹣1 , 溶液中的c(OH﹣)=molL﹣1 . 将SO2通入该氨水中,当c(OH﹣)降至1.0×10﹣7 molL﹣1时,溶液中的c(SO32﹣)/c(HSO3﹣)= .
【答案】
(1)降低反应活化能
(2)30℃、pH=2.0;蛋白质变性(或硫杆菌失去活性)
(3)H2SO4
(4)2OH﹣+SO2=SO32﹣+H2O;SO32﹣与Ca2+生成CaSO3沉淀,平衡向正向移动,有NaOH生成
(5)6.0×10﹣3;0.62
【解析】解:(1)4FeSO4+O2+2H2SO4 ![]() 2Fe2(SO4)3+2H2O,硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是做催化剂降低反应的活化能,
2Fe2(SO4)3+2H2O,硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是做催化剂降低反应的活化能,
所以答案是:降低反应活化能(或作催化剂);(2)从图象中分析可知,使用硫杆菌的最佳条件是亚铁离子氧化速率最大时,需要的温度和溶液pH分别为:30℃、pH=2.0,反应温度过高,反应速率下降是因为升温使蛋白质发生变性,催化剂失去生理活性,
所以答案是:30℃、pH=2.0; 蛋白质变性(或硫杆菌失去活性);(3)当 ![]() =4时,结合氧化还原反应电子守恒,4H2O2~4H2O~8e﹣ , 电子守恒得到H2S变化为+6价化合物,H2S~H2SO4~8e﹣ , 氧化产物的分子式为H2SO4 ,
=4时,结合氧化还原反应电子守恒,4H2O2~4H2O~8e﹣ , 电子守恒得到H2S变化为+6价化合物,H2S~H2SO4~8e﹣ , 氧化产物的分子式为H2SO4 ,
所以答案是:H2SO4 ;(4)过程①是二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,反应的离子方程式为:2OH﹣+SO2=SO32﹣+H2O,过程②加入CaO,存在CaO(s)+H2O (l)═Ca(OH)2(s)Ca2+(aq)+2OH﹣(aq),因SO32﹣与Ca2+生成CaSO3沉淀,平衡向正向移动,有NaOH生成,
所以答案是:2OH﹣+SO2=SO32﹣+H2O;SO32﹣与Ca2+生成CaSO3沉淀,平衡向正向移动,有NaOH生成;(5)NH3H2O的Kb=1.8×10﹣5 , 若氨水的浓度为2.0molL﹣1 , 由Kb= ![]() 可知c(OH﹣)=
可知c(OH﹣)= ![]() mol/L=6.0×10﹣3mol/L,
mol/L=6.0×10﹣3mol/L,
当c(OH﹣)降至1.0×10﹣7 molL﹣1时,c(H+)=1.0×10﹣7 molL﹣1 , H2SO3的Ka2=6.2×10﹣8 , 由Ka2= ![]() 可知c(SO32﹣)/c(HSO3﹣)=
可知c(SO32﹣)/c(HSO3﹣)= ![]() =0.62,
=0.62,
所以答案是:6.0×10﹣3;0.62.
【考点精析】掌握弱电解质在水溶液中的电离平衡和二氧化硫的污染及治理是解答本题的根本,需要知道当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理;SO2是污染大气的主要有害物质之一,直接危害是引起呼吸道疾病;形成酸雨pH<5、6,破坏农作物、森林、草原、使土壤酸性增强等等;含SO2的工业废气必须经过净化处理才能排放到空气中.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2 .
完成下列填空:
(1)化合物X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3﹣甲基﹣1,1,2,2﹣四溴丁烷.X的结构简式为 .
(2)异戊二烯的一种制备方法如图所示:
A能发生的反应有 . (填反应类型)
B的结构简式为 .
(3)设计一条由异戊二烯制得有机合成中间体 ![]() 的合成路线. (合成路线常用的表示方式为:A
的合成路线. (合成路线常用的表示方式为:A ![]() B…
B… ![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空. 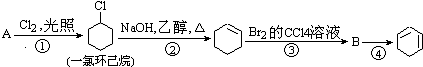
(1)A的结构简式是 , 名称是 .
(2)①的反应类型是 , ②的反应类型是 .
(3)反应④的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠是活泼金属的代表,钠和钠的化合物是中学化学的基础知识.请回答下列问题.
(1)钠跟水剧烈反应,生成和氢气(H2),此实验说明钠的化学性质活泼;
(2)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是;
(3)固体碳酸钠中含有碳酸氢钠杂质,除去该杂质的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2 , 充分反应后,向所得溶液中逐滴滴入1mol/L的盐酸溶液,所得气体的体积(标准状态)与所加盐酸的体积关系如图所示 
(1)写出OA段发生反应的离子方程式: .
(2)反应到B点时所得溶液中的溶质是 .
(3)原NaOH溶液的物质的量浓度是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组,拟探究和比较SO2和C12的漂白性,设计如图所示的实验装置二套.请你参与探究并回答下列问题. 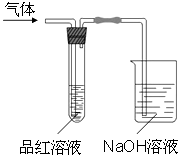
(1)向第一套装置中通入一段时间的SO2 , 观察到试管中的品红溶液褪色,然后再加热试管,溶液(填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12 , 观察到试管中的品红溶液也褪色,然后再加热试管,溶液(填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理(填“相同”或“不相同”);
(4)C12通入品红溶液中,生成的具有漂白性的物质是填“HC1”或“HClO”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)水中溶解氧是水生生物生存不可缺少的条件.某课外小组采用碘量法测定学校周边河水中的溶解氧.实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样.记录大气压及水体温度.将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2 , 实现氧的固定.
Ⅱ.酸化,滴定
将固氧后的水样酸化,MnO(OH)2被I﹣还原为Mn2+ , 在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32﹣+I2=2I﹣+S4O62﹣).
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是 .
(2)“氧的固定”中发生反应的化学方程式为 .
(3)Na2S2O3溶液不稳定,使用前需标定.配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除及二氧化碳.
(4)取100.00mL水样经固氧、酸化后,用a molL﹣1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为mgL﹣1 .
(5)上述滴定完成后,若滴定管尖嘴处留有气泡会导致测量结果偏 . (填“高”或“低”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com