
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | NaHCO3溶液与NaOH溶液反应:2OH-+2HCO3-═2 CO32-+H2O | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 钠和冷水反应 2Na+2H2O═2Na++2OH-+H2↑ |
分析 A.碳酸钙在离子反应中保留化学式;
B.反应生成碳酸钠和水,原子不守恒;
C.反应生成偏铝酸钠和水;
D.反应生成NaOH和氢气,遵循电子、电荷守恒.
解答 解:A.实验室用大理石和稀盐酸制取CO2的离子反应为CaCO3+2H+═Ca2++H2O+CO2↑,故A错误;
B.NaHCO3溶液与NaOH溶液反应的离子反应为OH-+HCO3-═CO32-+H2O,故B错误;
C.向AlCl3溶液中加入过量的NaOH溶液的离子反应为Al3++4OH-═AlO2-+2H2O,故C错误;
D.钠和冷水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+的电子排布图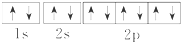 | |
| B. | Na+的结构示意图: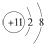 | |
| C. | 基态Na原子的电子排布式:1s22s22p53s2 | |
| D. | 基态Na原子的价电子排布式:3s1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1>△H2>△H3 | B. | △H1>△H3>△H2 | C. | △H3>△H2>△H1 | D. | △H2>△H1>△H3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BrCl和NaOH溶液反应生成NaCl、NaBrO两种盐 | |
| B. | BrCl具有较强的氧化性 | |
| C. | 能使润湿的淀粉碘化钾试纸变蓝 | |
| D. | BrCl与水反应中,BrCl既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+2NH${\;}_{4}^{+}$=Mg2++2NH3•H2O | |
| B. | 磷酸一氢钠溶液水解:HPO${\;}_{4}^{2-}$+H2O?PO${\;}_{4}^{3-}$+H3O+ | |
| C. | 电解AlCl3溶液:2Al${\;}_{3}^{+}$+6Cl-+6H2O$\frac{\underline{\;电解\;}}{\;}$2Al(OH)3↓+3H2↑+3Cl2↑ | |
| D. | 铜片接电正极,碳棒接电负极,电解硫酸溶液:Cu+2H+$\frac{\underline{\;电解\;}}{\;}$Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的质子数 | B. | 15N与14N是同种原子 | ||
| C. | 15N的核外电子数与中子数相同 | D. | 15N与14N互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com