
【题目】某铜矿石的主要成分是Cu2O,还含有少量的Al2O3、Fe2O3和SiO2。某工厂利用此矿石炼制精铜的工艺流程如图所示(已知:Cu2O+2H+=Cu+Cu2++H2O)。
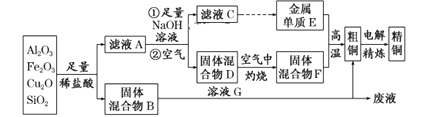
(1)滤液A中铁元素的存在形式为______________(填离子符号),生成该离子的离子方程式为_______________,检验滤液A中存在该离子的试剂为___________(填试剂名称)。
(2)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为____________________,在实验室中完成此实验还需要的试剂是________。
a.KClO3 b.KCl c.Mg d.MnO2
(3)为使固体混合物D在空气中灼烧完全分解,应_____________,直至连续两次测定的实验结果相同(或质量相差小于0.1g)时为止;灼烧时必须用到的实验仪器是__________。
(4)溶液G与固体混合物B反应的离子方程式为__________________________。
【答案】Fe2+ 2Fe3++Cu=2Fe2++Cu2+ 氯水和KSCN溶液(或双氧水和KSCN溶液等,合理即可) 2Al+Fe2O3![]() Al2O3+2Fe ac 灼烧,冷却至室温后称重,重复多次 坩埚 SiO2+2OH=SiO32+H2O
Al2O3+2Fe ac 灼烧,冷却至室温后称重,重复多次 坩埚 SiO2+2OH=SiO32+H2O
【解析】
向铜矿石中加足量稀盐酸发生的反应有:Al2O3+6HCl=2AlCl3+3H2O,Fe2O3+6HCl=2FeCl3+3H2O,Cu2O+2HCl=Cu+CuCl2+H2O, 2FeCl3+Cu=2FeCl2+CuCl2 ,因Cu2O是大量的,FeCl3完全转化为FeCl2。因此,固体混合物B的主要成分是Cu和SiO2,滤液A主要是CuCl2、AlCl3、FeCl2、HCl等混合溶液。滤液A中加足量NaOH溶液有反应:AlCl3+4NaOH=NaAlO2+2H2O+3NaCl,CuCl2+2NaOH=Cu(OH)2↓+2NaCl,FeCl2+2NaOH =Fe(OH)2↓+2NaCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以固体混合物D主要是Fe(OH)3和Cu(OH)2。D在空气中灼烧而分解2Fe(OH)3![]() Fe2O3+3H2O,Cu(OH)2
Fe2O3+3H2O,Cu(OH)2![]() CuO+H2O,故固体F是Fe2O3和CuO。滤液C主要是NaAlO2和NaCl溶液、NaOH溶液,根据“金属单质E+固体混合物F
CuO+H2O,故固体F是Fe2O3和CuO。滤液C主要是NaAlO2和NaCl溶液、NaOH溶液,根据“金属单质E+固体混合物F![]() 粗铜”可知金属单质E是铝。由“固体混合物B
粗铜”可知金属单质E是铝。由“固体混合物B![]() 粗铜”可知,加入溶液G是为了除去SiO2,显然溶液G可选用NaOH溶液:SiO2+2NaOH=Na2SiO3+H2O。金属Al分别与Fe2O3和CuO高温下发生铝热反应:Fe2O3+2Al
粗铜”可知,加入溶液G是为了除去SiO2,显然溶液G可选用NaOH溶液:SiO2+2NaOH=Na2SiO3+H2O。金属Al分别与Fe2O3和CuO高温下发生铝热反应:Fe2O3+2Al![]() 2Fe+Al2O3,3CuO+2Al
2Fe+Al2O3,3CuO+2Al![]() 3Cu+Al2O3,最后将粗铜作阳极电解精炼制得精铜。
3Cu+Al2O3,最后将粗铜作阳极电解精炼制得精铜。
(1)因为铜矿石中Cu2O是过量的,在稀盐酸中Cu2O+2HCl=Cu+CuCl2+H2O,生成的Cu能将溶液中FeCl3完全转化为FeCl2:2FeCl3+Cu=2FeCl2+CuCl2,向滤液A中先加KSCN溶液,溶液不变红色,排除了Fe3+存在,再加入氯水(或双氧水)后溶液变红色,可检验该溶液中含有Fe2+。所以滤液A中铁元素的存在形式为Fe2+。生成Fe2+的离子方程式为2Fe3++Cu=2Fe2++Cu2+,检验滤液A中存在Fe2+的试剂为KSCN溶液和氯水(或KSCN溶液和双氧水溶液);
(2)金属E是铝单质,固体F是Fe2O3和CuO的混合物,其中铝与Fe2O3在高温下反应可用于焊接钢轨,该反应的化学方程式为Fe2O3+2Al![]() 2Fe+Al2O3;因该反应是放热反应,且活化能较高,故需要高温引燃,KClO3和Mg作为引燃剂,答案选ac;
2Fe+Al2O3;因该反应是放热反应,且活化能较高,故需要高温引燃,KClO3和Mg作为引燃剂,答案选ac;
(3)固体混合物D中Fe(OH)3和Cu(OH)2空气中灼烧发生反应:2Fe(OH)3![]() Fe2O3+3H2O,Cu(OH)2
Fe2O3+3H2O,Cu(OH)2![]() CuO+H2O,若使之完全分解,应在坩埚中灼烧,冷却至室温后称重,重复多次,直至连续两次称量的结果相同且质量相差小于0.1g时为止;固体灼烧必须用到的实验仪器是坩埚;
CuO+H2O,若使之完全分解,应在坩埚中灼烧,冷却至室温后称重,重复多次,直至连续两次称量的结果相同且质量相差小于0.1g时为止;固体灼烧必须用到的实验仪器是坩埚;
(4)从流程图上看,固体混合物B中含有SiO2和Cu,加入溶液G是为了回收混合物B中的Cu,溶液G如果是NaOH溶液,即可将SiO2转化为易溶于水的Na2SiO3,再过滤即可得到Cu,其反应的离子方程式为SiO2+2OH-=SiO32-+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是![]()
A.金刚石、SiC、NaF、NaCl、![]() 、
、![]() 晶体的熔点依次降低
晶体的熔点依次降低
B.CaO晶体结构与NaCl晶体结构相似,CaO晶体中![]() 的配位数为6,且这些最邻近的
的配位数为6,且这些最邻近的![]() 围成正八面体
围成正八面体
C.设NaCl的摩尔质量为![]() ,NaCl的密度为
,NaCl的密度为![]() ,阿伏加德罗常数为
,阿伏加德罗常数为![]()
![]() ,在NaCl晶体中,两个距离最近的
,在NaCl晶体中,两个距离最近的![]() 中心间的距离为
中心间的距离为
D.X、Y可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角位置,则该晶体的化学式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锌电池在商业、宇航潜艇、核武器等领域有广泛应用。一种从正极片(含Ag、Ag2O、石墨及Cu等)中回收银的流程如下,下列叙述错误的是
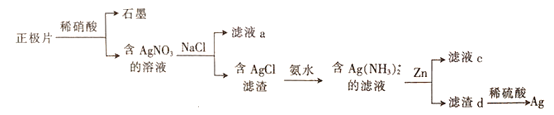
A. 滤液a中含有Na+、Cu2+、H+等阳离子
B. A用氨水溶解时发生的反应为AgCl+2NH3H2O=[Ag(NH3)2]++C1-+2H2O
C. 滤液c可浓缩结晶得到Zn(NO3)2
D. 向滤渣d中加稀硫酸可溶解其中过量的Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①盐卤(含MgCl2)![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液
MgCl2溶液![]() 无水MgCl2
无水MgCl2
②铝土矿![]() AlO2-
AlO2-![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3
③NH3![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
④NaCl溶液![]() Cl2
Cl2![]() 无水FeCl2
无水FeCl2
⑤S![]() SO3
SO3![]() H2SO4
H2SO4
⑥SiO2![]() Na2SiO3溶液
Na2SiO3溶液![]() H2SiO3
H2SiO3
A. ③⑥B. ③⑤⑥C. ①④⑤D. ①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如图所示:
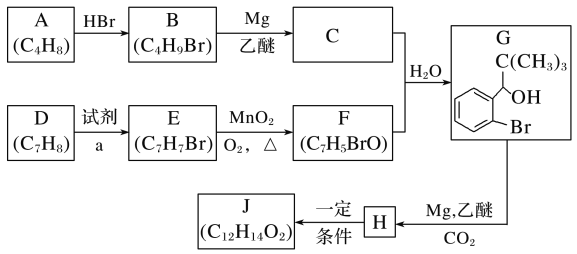
已知:
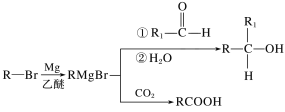
(1)B的化学名称是__,F中官能团名称是__。
(2)由E生成F的反应类型是__,由H生成J的反应类型是__。
(3)试剂a是__。
(4)J是一种环酯,则J的结构简式为__。H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为__。
(5)利用题中信息写出以乙醛和苯为原料,合成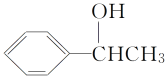 的流程图(其他试剂自选)___。
的流程图(其他试剂自选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和化学平衡影响的图像,其中图像和实验结论表达正确的是
A.a是其他条件一定时,反应速率随温度变化的图像,正反应![]()
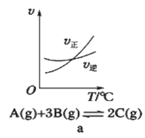
B.b是在有无催化剂存在下建立的平衡过程图像,Ⅰ是使用催化剂时的曲线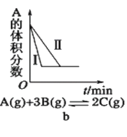
C.c是一定条件下,向含有一定量A的容器中逐渐加入B时的图像![]() 纵坐标为C的物质的量分数
纵坐标为C的物质的量分数![]() ,压强
,压强![]()
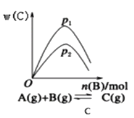
D.d是在平衡体系的溶液中加入少量FeCl3固体的化学反应速率随时间变化的图像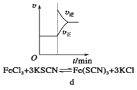
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素![]() 、
、![]() 、
、![]() 、
、![]() 的原子序数依次增大,
的原子序数依次增大,![]() 的原子在元素周期表中半径最小;
的原子在元素周期表中半径最小;![]() 的次外层电子数是其最外层电子数的
的次外层电子数是其最外层电子数的![]() ;
;![]() 的单质可与冷水剧烈反应,产生
的单质可与冷水剧烈反应,产生![]() 的单质;
的单质;![]() 与
与![]() 属于同一主族。下列叙述正确的是
属于同一主族。下列叙述正确的是
A.![]() 元素形成的简单离子与
元素形成的简单离子与![]() 元素形成的简单离子的核外电子总数相同
元素形成的简单离子的核外电子总数相同
B.单质的氧化性:![]()
C.化合物![]() 、
、![]() 、
、![]() 中化学键的类型完全相同
中化学键的类型完全相同
D.原子半径:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z、W的原子序数依次增加。m、P、r是由这些元素组成的二元化合物,n是W的单质,q是Y的单质,s是Z的单质且常温下为淡黄色固体,m 与r相遇会产生白烟。上述物质的转化关系如图所示。下列说法错误的是

A. 原子半径:z>W>X
B. Y的一种氢化物可作为制冷剂
C. Z的氧化物对应的水化物酸性一定比W的弱
D. X、Y、W三种元素组成的化合物可为离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】放热反应CO(g)+H2O(g)CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0mol·L-1,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则( )
A.K2和K1的单位均为mol·L-1B.K2<K1
C.c2(CO)>c2(H2O)D.c1(CO)>c2(CO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com