


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.1∶2∶3 | B.3∶1∶1 | C.6∶3∶2 | D.1∶1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢氧根离子的摩尔质量是17g |
| B.每mol硫酸所含硫酸的分子数为6.02×1023/mol |
| C.物质的量浓度相同的溶液中,所含溶质的微粒数相同 |
| D.0.1 mol氯化氢约含有6.02×1022个氯化氢分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. Na参加氧化还原反应时电子转移NA Na参加氧化还原反应时电子转移NA |
B. 与 与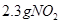 所含有的氧原子数相等 所含有的氧原子数相等 |
C.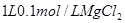 溶液中 溶液中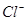 离子数为 离子数为 |
D.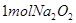 与足量水反应后转移的电子数为2NA 与足量水反应后转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.100ml 1mol/LNaCl溶液 | B.75ml 1mol/LMgCl2溶液 |
| C.150ml 3mol/LKCl溶液 | D.25ml 2mol/LAlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.7∶5 | B.3∶7 | C.7∶1 | D.1∶7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.10ml | B.25ml | C.50ml | D.100ml |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com