
����Ŀ�����ú�̼������ϳ���ȼ���Ƿ�չ��̼���õ���Ҫ��������֪��CO(g) + 2H2(g)![]() CH3OH(g)�Ǻϳɼ״���CH3OH���ķ�Ӧ���÷�Ӧ���̵������仯��ͼ��ʾ�������ж���ȷ���ǣ� ��
CH3OH(g)�Ǻϳɼ״���CH3OH���ķ�Ӧ���÷�Ӧ���̵������仯��ͼ��ʾ�������ж���ȷ���ǣ� ��
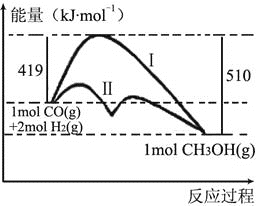
A. CO��g����H2��g����Ӧ����1mol CH3OH��g���ͷų�91kJ������
B. ��̼�Ʊ�ԭ����CO��H2�ķ�Ӧ���ڷ��ȷ�Ӧ
C. ��Ӧ���ܼ��ܸ�����������ܼ���
D. ���÷�Ӧ����Һ̬CH3OH����ų�����������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʽṹ�����ʡ�A��B��C��DΪԭ�������������������Ԫ�أ�A2-��B+������ͬ�ĵ��ӹ��ͣ�C��DΪͬ����Ԫ�أ�C�������������������������3����DԪ���������һ��δ�ɶԵ��ӡ��ش��������⣺
��1������Ԫ���е縺��������____(��Ԫ�ط���)������Cԭ�ӵĺ�������Ų�ʽΪ______________��
��2������A������ͬ�������壬���зе�ߵ���___________(�����ʽ)��ԭ����_________________��A��B���⻯�������ľ������ͷ�Ϊ______________��______________��
��3��C��D��Ӧ��������ɱ�1:3�Ļ�����E��E�����幹��Ϊ________________������ԭ�ӵ��ӻ��������___________________��
��4��������D2A�����幹��Ϊ______________������ԭ�ӵļ۲���Ӷ���Ϊ_______________������D��ʪ���Na2CO3��Ӧ���Ʊ�D2A���仯ѧ����ʽΪ_____________________��
��5��A��B�ܹ��γɻ�����F���侧���ṹ��ͼ��ʾ����������a=0.566nm��F�Ļ�ѧʽΪ_________��������Aԭ�ӵ���λ��Ϊ__________����ʽ���㾧��F���ܶ�_____________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NO ��CO2 ��N2O4��������ֱ���0.5 mol��ԭ�ӣ�������������ʵ���֮��Ϊ�� ��
A. 1:1:2 B. 4:2:1 C. 1:1:1 D. 1:2:4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ҵ�ijЩ���������ʾ��
���� | �۵㣨�棩 | �е㣨�棩 | �ܶȣ�g/mL�� | ˮ�е��ܽ��� |
�� | -98 | 37.5 | 0.93 | ���� |
�� | -48 | 95 | 0.90 | ���� |
���м��ҵĻ������з���ʱ���ɲ��õķ����ǣ� ��
A.����B.����C.����D.��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������ת��������AΪ����������CΪ�
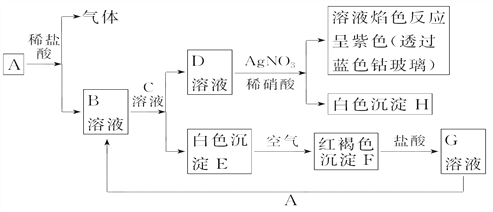
�Իش�
��1��д��F�Ļ�ѧʽ________��H�Ļ�ѧʽ___________________________________��
��2��д����Eת���F�Ļ�ѧ����ʽ��________________________________��
��3����G��Һ����A���йط�Ӧ���ӷ���ʽ��________________________________________��
��4��д��A��һ����������ˮ��Ӧ�Ļ�ѧ����ʽ��_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ��������������������ε��ǣ� ��
A.Na2SO4B.Ca(NO3)2C.NaNO3D.CH3COONa
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�1���ˮ�ܽ�700���������������Һ�ܶ�Ϊ0.9gcm��3 �� ���ְ�ˮ�����ʵ���Ũ�Ⱥ����ʵ����������ֱ�Ϊ�� ��
A.18.4molL��134.7%
B.20.4molL��138.5%q2
C.18.4molL��138.5%
D.20.4molL��134.7%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и��������У�Y������X��Ӧ������Z��Ӧ����
X | Y | Z | |
�� | NaOH��Һ | NH4HCO3 | ϡ���� |
�� | KOH��Һ | SO2 | Ũ���� |
�� | O2 | N2 | H2 |
�� | FeCl3��Һ | Cu | Ũ���� |
A.�٢�B.�٢�C.�ڢ�D.�ڢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com