
【题目】下图为电解饱和食盐水的实验装置。据此,下列叙述不正确的是 ( )
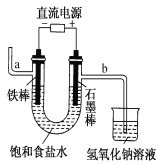
A.装置中a管能产生氢气
B.b管导出的是能使湿润的淀粉碘化钾试纸变蓝的气体
C.在石墨棒电极区域有NaOH生成
D.以电解饱和食盐水为基础制取氯气等产品的工业称为“氯碱工业”
【答案】C
【解析】
根据图知,Fe作阴极、石墨棒作阳极,Fe电极反应式为2H2O+2e- =H2↑+2OH -,石墨棒电极反应式为2Cl- -2e- =Cl2↑,则a得到的气体是氢气、b管导出的气体是氯气,Fe棒附近有NaOH生成,据此分析解答。
A.根据图知, Fe作阴极、石墨棒作阳极,Fe电极反应式为2H2O+2e- =H2↑+2OH - ,石墨棒电极反应式为2Cl- -2e- =Cl2↑,则a得到的气体是氢气、b管导出的气体是氯气,选项A正确;
B .根据A知,b管导出的气体是氯气,选项B正确;
C .根据A知阴极氢离子放电,破坏水的电离平衡,Fe电极附近有NaOH生成,石墨电极附近没有NaOH生成,选项C错误;
D .该电解池电解过程中有氯气、氢气和NaOH生成,所以以食盐水为基础原料制取氯气等产品的工业称为"氯碱工业”,选项D正确;
答案选C。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某学生需要用烧碱固体配制0.5mol·L-1的NaOH溶液480mL。实验室提供以下仪器:
①100mL烧杯 ②100mL量筒 ③1000mL容量瓶 ④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码) ⑦药匙。请回答下列问题:
(1)计算需要称取NaOH固体_________g。
(2)配制时,必须使用的仪器有_______(填代号),还缺了仪器名称是_________。
(3)配制时,其正确的操作顺序是(字母表示,每个操作只用一次)________。
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)若出现如下情况,其中将引起所配溶液浓度偏高的是___。(填下列编号)
①容量瓶实验前用蒸馏水洗干净,但未烘干 ②定容观察液面时俯视
③配制过程中遗漏了(3)中步骤A ④加蒸馏水时不慎超过了刻度
⑤未等NaOH溶液冷却至室温就转移到容量瓶中
(5)用配制好的溶液,再来配制50ml0.2mol·Lˉ1的NaOH溶液,需要取原配好的溶液_____ml。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种元素,已知:①X、Y、Z的单质在常温下均为气体;②X单质可在Z单质中燃烧,生成XZ,火焰为苍白色;③XZ极易溶于水,其水溶液可使蓝色石蕊试纸变红;④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为液体;⑤Z单质溶于X2Y中,所得溶液具有漂白作用;⑥细铁丝能在Z2(g)中剧烈燃烧,且产生红棕色烟。推断:
(1)X、Y两种元素的名称X___,Y___。
(2)化合物的化学式:XZ___,X2Y___。
(3)过程⑥中涉及的化学反应方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对![]() 的性质进行探究,设计了以下实验
的性质进行探究,设计了以下实验

已知:![]() 、
、![]() 、
、![]() 等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是
等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是
A.溶液颜色变红时发生反应的离子方程式是:![]()
B.红色溶液褪色表现了![]() 的漂白性
的漂白性
C.氧化性:![]()
D.无色溶液Ⅱ中滴入适量的![]() 溶液,溶液又变成红色
溶液,溶液又变成红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为1 NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C. 常温常压下,1 NA 个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol·L-1 NaOH溶液滴定20.00mL 0.1000 mol·L-1某酸(HA)溶液,溶液中HA、A-的物质的量分数δ(X)随pH的变化如图所示。[已知δ(X)=![]() ]下列说法正确的是
]下列说法正确的是
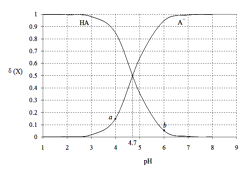
A.Ka(HA)的数量级为10-5
B.溶液中由水电离出的c(H+):a点>b点
C.当pH=4.7时,c(A-)+c(OH-)=c(HA)+c(H+)
D.当pH=7时,消耗NaOH溶液的体积为20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要1.500 mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:
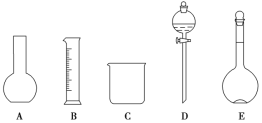
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制450 mL 1.50 mol·L-1的稀硫酸。计算所需浓硫酸的体积为________ mL (保留1位小数),现有 ①10 mL ②25 mL ③50 mL ④100 mL四种规格的量筒,最好选用的量筒是________(填代号)。
(3)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为:②→①→③→___→_____→_____→______→④(填序号)。
(4)在配制过程中,下列操作中会导致所配制的溶液浓度偏高的有________。
①用量筒量取浓硫酸时候,俯视刻度线
②洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍、钴、钛、铜等元素常用作制备锂离子电池的正极材料或高效催化剂。NA表示阿伏加德罗常数,请填写下列空白。
(1)基态Co原子的电子排布式为___。
(2)镍与CO生成的配合物Ni(CO)4中,易提供孤电子对的成键原子是___(填元素名称);1 molNi(CO)4中含有的σ键数目为__;写出与CO互为等电子体的一种阴离子的化学式_____。
(3)Ti(BH4)2是一种储氢材料。BH4-的空间构型是____,B原子的杂化方式__。与钛同周期的第ⅡB族和ⅢA族两种元素中第一电离能较大的是___(写元素符号),原因是____。
(4)CuFeS2的晶胞如图所示,晶胞参数分别为anm、bnm、cnm;CuFeS2的晶胞中每个Cu原子与___个S原子相连,晶体密度ρ=___g·cm3(列出计算表达式)。

以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子2和3的坐标分别为(0,1,![]() )、(
)、(![]() ,
,![]() ,0),则原子1的坐标为___。
,0),则原子1的坐标为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com