
 +H2O→MnO
+H2O→MnO +SO
+SO +H+,下列说法不正确的是( )
+H+,下列说法不正确的是( )| A.可以利用该反应检验Mn2+ |
| B.配平后的系数为2、5、8、2、10、16 |
| C.该反应中酸性介质不能为盐酸 |
| D.若有0.1mol还原产物生成, 则转移电子0.5mol |
科目:高中化学 来源:不详 题型:单选题
| A.Li2NH中N的化合价是-1 | B.该反应中H2既是氧化剂又是还原剂 |
| C.储存1mol H2 时转移的电子为2mol | D.此法储氢和钢瓶储氢的原理相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O
2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O| A.反应①和⑤都属于置换反应 |
| B.MoO3属于碱性氧化物 |
| C.在反应①中Mo和S均被氧化 |
| D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为2:2:3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> I2。 |
| B.①中Se是氧化产物,I2是还原产物 |
| C.反应①中KI是氧化剂,SeO2是还原剂 |
| D.反应①中每有1.0 mol I2生成,转移电子数目为4NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤ | B.②④⑤ | C.①②③⑤ | D.①③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述反应中氧化剂和还原剂的物质的量之比为5:6 |
| B.产生白色烟雾的原因是生成的P205白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)形成气溶胶 |
| C.上述反应中消耗3 mol P时,转移电子的物质的量为15mol |
| D.因红磷和白磷互为同素异形体,所以上述火药中的红磷可以用白磷代替 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
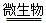 4H++2Fe2++________;
4H++2Fe2++________;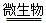 4Fe3++____________;
4Fe3++____________;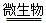 3Fe2++2S;
3Fe2++2S;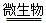 4H++2SO42—。
4H++2SO42—。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分解反应一定是氧化还原反应 |
| B.非金属单质在氧化还原反应中一定作氧化剂 |
| C.氧化剂具有氧化性,还原剂具有还原性 |
| D.氧化剂在氧化还原反应中被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com