
下列说法正确的是
| A.阴阳离子通过静电吸引形成离子键 |
| B.HF、HCl、HBr、HI的热稳定性和还原性均依次减弱 |
| C.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
科目:高中化学 来源: 题型:单选题
关于下列各组物质的相互关系,判断正确的是( )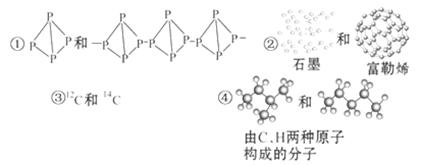

| A.互为同素异形体的是①② | B.互为同位素的是②③ |
| C.互为同一物质的是①⑤ | D.互为同分异构体的是④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z在元素周期表中的位置如图所示,其中Y与Z的原子最外层电子数之比为2:1.下列说法不正确的是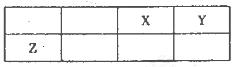
| A.X与Y只能形成两种化台物 |
| B.简单离子的半径大小:Y<X |
| C.X、Y、Z三种元素形成的化合物中既存在共价键又存在离子键 |
| D.Z形成的简单离子是其所在周期元素形成的简单离子中半径最小的 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.元素周期表中一共有7个周期和18个族 |
| B.金属元素的原子最外层电子数一定都小于4 |
| C.质量数不同的两种原子,一定不互为同位索 |
| D.主族元素X的原子序数为a,所在周期的元素种数为b,则与x同族的下一周期的元素Y的原于序数一定为a+b |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学学习中,推理是一种重要的学习方法,下列推论正确的是
A.由“BF3和SO3互为等电子体”,可推知二者均为非极性分子
B.由“同主族元素性质相似,CO2为直线形分子”,可推知SiO2为直线形分子
C.由“SiH4的熔沸点比CH4高”,可推知PH3的熔沸点比NH3高
D.由“C、N、O三种元素的电负性C<N<O”,可推知第一电离能C<N<O
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是
| A.原子序数: X<Y | B.原子半径:X<Y |
| C.离子半径:X>Y | D.原子最外层电子数:X<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
最近,意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子O4,并用质谱仪探测到了它存在的证据。下列说法正确的是
| A.O4是氧元素的一种同位素 |
| B.O4可能含有极性键 |
| C.同温同压下,等体积的O4气体和O2含有相同的分子数 |
| D.O4转化O2为物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z- ,Y+和Z-离子具有相同的电子层结构。下列说法正确的是( )
| A.原子最外层电子数:X>Y>Z | B.单质沸点:X>Y>Z |
| C.离子半径:X2->Y+>Z- | D.原子序数:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
镭是元素周期表中第七周期第ⅡA族元素,下列关于镭的性质描述不正确的是( )
| A.在化合物中呈+2价 | B.单质能与水反应放出氢气 |
| C.镭比钙的金属性弱 | D.碳酸镭难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com