
����Ŀ����14�֣�ij����ャҺ����Al(OH)3��MnO2������Na2CrO4,�����ǵ��������������ʹNa2CrO4������ȫ��ˮ������ij�о�С��������Ƶĵ�����װ�ã���ͼ2����ʹ��Һ����ɹ�������ͺ���Ԫ����Һ�����������á��ش��͢��е����⡣ 
��������ķ�������ã�����ͼ�еIJ��ַ�������ͷ�Ӧ����δ������
��1����Ӧ�������Լ�NaOH�ĵ���ʽΪ��B��C�ķ�Ӧ����Ϊ �� C��Al���Ʊ�������Ϊ��
��2����С��̽����Ӧ�ڷ�����������D��Ũ�����ϣ������ȣ��ޱ仯��������Cl2���ɣ�����Ӧֹͣ������ʣ�࣬��ʱ�μ����ᣬ�ֲ���Cl2���ɴ��ж�Ӱ��÷�Ӧ��Ч���е������У�����ţ��� a���¶� b��Cl-��Ũ�� c����Һ�����
��3��0.1 mol Cl2�뽹̿��TiO2��ȫ��Ӧ������һ�ֻ�ԭ�������һ����ˮ���TiO2��xH2O��Һ̬���������4.28 kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ��
��4������Ԫ����Һ�ķ�������� �ö��Ե缫���ʱ�� ![]() �ܴӽ�Һ�з��������ԭ���� �� �����Ԫ�ص������������������ɵ�����Ϊ��д��ѧʽ����
�ܴӽ�Һ�з��������ԭ���� �� �����Ԫ�ص������������������ɵ�����Ϊ��д��ѧʽ����
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����70g��������������ƵĻ����Ͷ�뵽100gˮ�У����õ�����Һ������Ϊ162g����ԭ������������Ƶ�����Ϊ__________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ASES��˾��Ƶ�����������DZͧ��Һ����Һ��ȼ�ϵ��ʾ��ͼ��ͼ��ʾ�������й�˵����ȷ���ǣ� �� 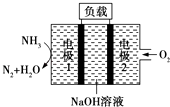
A.��ع���ʱ��Na+��缫1�ƶ�
B.��ع���һ��ʱ���ֹͣ����ҺPHֵ�ȿ�ʼʱ���Լ�С
C.�缫1�����ĵ缫��ӦΪ2NH3+6OH����6e���TN2��+6H2O
D.�øõ������Դ��⾫��ͭ��������ÿ����0.2 mol NH3��ͬʱ������õ�19.2g��ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʰ��ᡢ��Ρ��л�������˳�����е���
A. ���ᡢ�����ơ����������Ȼ�̼����ˮ
B. ̼�����ơ���ʯ�ҡ�ʳ�Ρ��ƾ����Ͻ�
C. ���ᡢ���̼��ơ�����ʯ��||
D. ���ᡢ��ʯ�ҡ�������ء����顢ʯ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѹ���ʻ�������������ԭ��Ϊ��Ni(s)+4CO(g) ![]() Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�棬�������ʲ����뷴Ӧ�� ��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�棬�������ʲ����뷴Ӧ�� ��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
�ڶ��Σ�����һ�η�Ӧ���������������������230���Ƶøߴ�����
�����ж���ȷ���ǣ� ��
A.����c(CO)��ƽ���������ƶ�����Ӧ��ƽ�ⳣ������
B.��һ�Σ���30���50������֮��ѡ��Ӧ�¶ȣ�ѡ50��
C.�ڶ��Σ�Ni(CO)4�ֽ��ʽϵ�
D.�÷�Ӧ�ﵽƽ��ʱ��v����[Ni(CO)4]=4v����(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪTʱ����4.0L�����ܱ������г���2.0mol PCl5 �� ������Ӧ��PCl5��g��PCl3��g��+Cl2��g������Ӧʱ�䣨t����������������ѹǿ��p�������ݼ�����
t/s | 0 | 50 | 150 | 250 | 350 |
��ѹǿp/100kPa | 100 | 116 | 119 | 120 | 120 |
��1������ѹǿp����ʼѹǿp0���㷴Ӧ��PCl5��ת���ʦ���PCl5���ı���ʽΪ��ƽ��ʱPCl5��ת����Ϊ���٣�
��2����Ӧ��ǰ50s��ƽ������v��PCl3��Ϊ���٣�
��3�����¶��µ�ƽ�ⳣ��Ϊ���٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ijBa��OH��2��Һ����μ���pH=x�����ᣬ��û����Һ�IJ���pH�����ʾ��
��� | ����������Һ�����/mL | ��������/mL | ��Һ��pH |
�� | 22.00 | 0.00 | 13 |
�� | 22.00 | 18.00 | 12 |
�� | 22.00 | 22.00 | 7 |
��1��Ba��OH��2��Һ�����ʵ���Ũ��Ϊ��
��2��x��ֵ�Ƕ��٣�
��3����100mL����Ba��OH��2��Һ����μ���0.05mol/L NaHCO3��Һ���������պô����ֵʱ��Һ��pHΪ���٣�����֪lg2=0.3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������SO2ͨ�벻ͬ��Һ��ʵ���������ý��۲���ȷ���ǣ� ��
ʵ�� | ���� | ���� | |
A | ��HCl��BaCl2�� | ������ɫ���� | SO2�л�ԭ�� |
B | H2S��Һ | ������ɫ���� | SO2�������� |
C | ����KMnO4��Һ | ��ɫ��Һ��ɫ | SO2��Ư���� |
D | Na2SiO3��Һ | ������״���� | ���ԣ�H2SO3>H2SiO3 |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҩƷ˵�����б�����ÿ�˺���15mg��þ65mg ��ͭ2mg��п1.5mg����1mg���˴�����ɷ���ָ
A.����B.ԭ��C.����D.Ԫ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com