
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L-1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
【答案】C
【解析】由n是元素Z的单质,通常为黄绿色气体,可知Z元素为Cl,n为Cl2,再根据q的水溶液具有漂白性,可知q为HClO,由0.01 mol·L-1 r溶液的pH为2,可判断r为一元强酸,则r为HCl,然后根据n和p的反应条件,以及s通常是难溶于水的混合物,可知p为烷烃,s为烷烃的氯代物;根据题意,W、X、Y、Z是短周期原子序数依次增加的四种元素,可进一步推知W、X、Y、Z分别为H、C、O、Cl。A、根据原子半径的变化规律,可知原子半径:H<O<C,选项A错误;B、根据同周期元素非金属的变化规律,可知非金属性:O>C,再由CCl4、ClO2中化合价的正负,可知非金属性:O>Cl>C,选项B错误;C、氧的氢化物可能为H2O或H2O2,常温常压下二者均为液态,选项C正确;D、碳的最高价氧化物的水化物H2CO3为弱酸,选项D错误。答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1) 19.2g SO2在标准状况下的体积为___________L,其中含氧原子的物质的量为_______mol,该气体在标准状况下的密度是______________。
(2)0.5mol H3PO4的质量是_______g,含______个H3PO4分子,含______mol氧原子
(3)在标准状况下,将_______L NH3溶于水得到0.5 mol·L-1的氨水500 mL;配制100 mL 0.1 mol·L-1CuSO4溶液,需要CuSO4·5H2O________g。
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
①同温同压下,M、N气体的密度之比为____________;
②相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 钠燃烧时发出黄色火焰
B. 在常温下,铝不能与氧气反应
C. 常温下可以用铁罐装运浓硫酸
D. 为了检验某FeCl2溶液是否变质,可向溶液中加入KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生成锂离子电池。下列说法正确的是
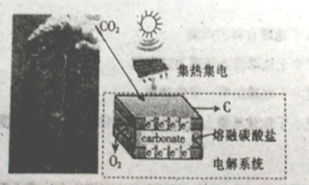
A. 图中能量转化方式只有一种
B. 阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑
C. 若反应中转移1mole-,则理论上消耗CO32-0.5mol
D. 当生成12g碳材料时,可收集到22.4LO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有NaCl和KCl的混合物25g,溶于水形成溶液,加入1000g 7.14%的AgNO3溶液,充分反应后滤出沉淀,再向混合物加入100g Cu片,过一段时间取出(反应完全),洗涤干燥称其质量为101.52g,求原混合物中NaCl和KCl的物质的量各为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法中正确的是( )
A.凡是含碳元素的化合物都属于有机物
B.易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物
C.所有的有机物都很容易燃烧
D.有机物不一定都不溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是

A. a为电池的正极,发生还原反应
B. b极的电极反应为HCHO+H2O-4e-==CO2+4H+
C. 传感器工作过程中,电解质溶液中硫酸的浓度减小
D. 当电路中转移2×10-4 mol电子时,传感器内参加反应的HCHO为3.0 mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com