
【题目】用如图所示装置进行如下实验,能达到实验目的的是( )
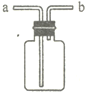
A.瓶中盛满水,从b口进气,用排水法收集NO2
B.瓶中盛适量浓硫酸,从a口进气干燥NH3
C.从b口进气,用排空气法收集CO2
D.瓶中装满水,a口连接导管并伸入量筒中,从b口进气,测量生成H2的体积
科目:高中化学 来源: 题型:
【题目】硫酸生产中炉气转化反应为:2SO2(g)+O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
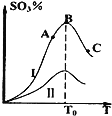
A.该反应的正反应为放热反应
B.曲线Ⅰ上A、C两点反应速率的关系是:vA>vC
C.反应达到B点时,2v正(O2)= v逆(SO3)
D.已知V2O5的催化效果比Fe2O3好,若Ⅰ表示用V2O5作催化剂的曲线,则Ⅱ可表示为Fe2O3作催化剂的曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照要求写出化学方程式
(1)乙烯发生聚合反应:_____________________________________________
(2)苯与浓硝酸反应:_____________________________________________
(3)乙醇和乙酸的酯化反应:___________________________________________
(4)乙醇消去反应制乙烯:______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。将变黑的银质器皿放入下图装置,一段时间后发现黑色会褪去。回答下列问题:
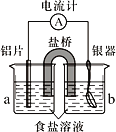
(1)铝为________极,KNO3盐桥中的________离子进入a烧杯中,银器的电极反应式为________。
(2)如不用盐桥,将铝片和银器插入一个盛食盐水的烧杯中处理,负极的电极反应式是_________,总反应方程式_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应a A(g)+b B(s)![]() c C(g)+d D(g)达平衡后,保持温度不变,将容器缩小为原来的一半,达到新的平衡时,A的浓度是原来的1.6倍,则下列说法正确的是
c C(g)+d D(g)达平衡后,保持温度不变,将容器缩小为原来的一半,达到新的平衡时,A的浓度是原来的1.6倍,则下列说法正确的是
A. 平衡向逆反应方向移动B. a<c+d
C. 物质A的转化率增大D. 物质D的浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同体积、相同pH的氨水和氢氧化钠溶液加水稀释时的pH变化曲线如下图所示,下列判断正确的是
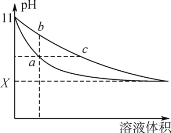
A. b点溶液导电能力比a点溶液强
B. 对于b、c两点,电离平衡常数Kb>Kc
C. 与盐酸完全反应时,消耗盐酸体积:Va>Vc
D. X的值接近7,但大于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TK时,向2.0 L恒容密闭容器中充入0.10 mol COCl2,发生反应COCl2(g)![]() Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
下列说法正确的是
A. 保持其他条件不变,升高温度,平衡时c(Cl2)=0.022 mol·L-1,则反应的ΔH<0
B. 反应在前2 s的平均速率v(CO)=0.015 mol·L-1·s-1
C. 保持其他条件不变,起始向容器中充入0.12 mol COCl2、0.06 mol Cl2和0.06 mol CO,反应达到平衡前的速率:v正<v逆
D. 保持其他条件不变,起始向容器中充入0.10 mol Cl2和0.08 mol CO,达到平衡时,Cl2的转化率小于60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧硫酸氢钾复合盐(K2SO4KHSO42KHSO5)易分解,可用作漂白剂、NOx和SO2等的脱除剂。某研究小组制备过氧硫酸氢钾复合盐的流程如图所示。

已知:浓硫酸与H2O2反应,部分转化为过硫酸(化学式为H2SO5,是一种一元强酸)
(1)H2SO5中硫元素的化合价为+6价,其中过氧键的数目为________;工业上用过氧硫酸氢钾复合盐溶液脱除NO时,反应的离子方程式为___________________________。
(2)若反应物的量一定,在上述流程的“转化”步骤中需用冰水浴冷却,且缓慢加入浓硫酸,其目的是___________________________。
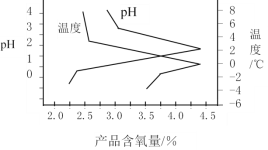
(3)“结晶”操作中,加入K2CO3即可获得过氧硫酸氢钾复合盐晶体,该过程的化学方程式为______________________________。过氧硫酸氢钾复合盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如图所示,则该过程适宜的条件是_________________。
(4)产品中KHSO5含量的测定:取1.000g产品于锥形瓶中,用适量蒸馏水溶解,加入5mL5%的硫酸和5mL25%的KI溶液,再加入1mL淀粉溶液作指示剂,用0.2000mol·L-1硫代硫酸钠标准液滴定至终点,消耗标准液的体积为25.00mL。
已知:2KHSO5+4KI+H2SO4 = 2I2+3K2SO4+2H2O I2+2Na2S2O3 =Na2S4O6+2NaI
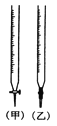
①用_____滴定管盛装标准浓度的硫代硫酸钠溶液(填“甲”或“乙”)。
②产品中KHSO5的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是有机合成中的部分片段:
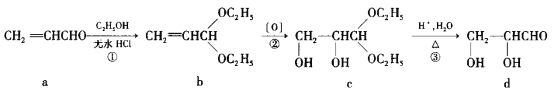
下列说法错误的是
A.有机物a能发生加成、氧化、取代等反应
B.有机物a~d都能使酸性高锰酸钾溶液褪色
C.d中所有原子不可能共平面
D.与b互为同分异构体、含有1个![]() 和2个
和2个![]() 的有机物有4种
的有机物有4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com